
 红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.
红葡萄酒密封储存时间越长,质量越好,原因之一是储存过程中生成了酯.在实验室也可以用如图所示的装置制取乙酸乙酯,请回答下列问题.分析 (1)-COOH为羧酸的官能团,名称为羧基;
(2)乙醇、乙酸易溶于水,饱和碳酸钠溶液可降低乙酸乙酯的溶解度,导管在液面下可发生倒吸;
(3)酯化反应中,浓硫酸作催化剂可加快反应速率,作吸水剂可使反应正向移动;
(4)乙醇与乙酸发生酯化反应生成乙酸乙酯、水,属于取代反应;
(5)酯的密度小于水,不溶于水,具有香味.
解答 解:(1)乙酸分子中-COOH原子团的名称是羧基,故答案为:羧基;
(2)装置b中通蒸气的导管应置于饱和碳酸钠溶液的液面上而不能插入溶液中,目的是防止倒吸,故答案为:防止倒吸;
(3)浓硫酸的作用是催化剂、吸水剂,故答案为:催化剂;吸水剂;
(4)试管 a 中发生反应的化学方程式为CH3CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O,反应类型为取代反应,
故答案为:CH3CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$CH3COOC2H5+H2O;取代反应;
(5)反应时生成的乙酸乙酯密度比水小,可以闻到香味,故答案为:小;香.
点评 本题考查乙酸乙酯的制备实验,为高频考点,把握官能团与性质、有机反应、实验技能为解答的关键,侧重分析与实验能力的考查,注意浓硫酸的作用及混合物分离提纯,题目难度不大.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.
肉桂酸是香料、化妆品、医药、塑料和感光树脂等的重要原料.实验室用下列反应制取肉桂酸.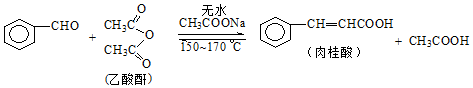
| 苯甲醛 | 乙酸酐 | 肉桂酸 | 乙酸 | |
| 溶解度(25℃,g/100g水) | 0.3 | 遇热水水解 | 0.04 | 互溶 |
| 沸点(℃) | 179.6 | 138.6 | 300 | 118 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com