
| A. | 能与NaOH溶液反应 | |
| B. | 能使品红溶液褪色 | |
| C. | 见光能分解 | |
| D. | 向Ca(ClO)2 溶液中通入CO2能生成次氯酸 |
分析 部分电离的电解质是弱电解质,要证明次氯酸是弱酸,只要证明次氯酸部分电离即可,据此分析解答.
解答 解:A.次氯酸和NaOH溶液反应生成次氯酸钠和水,说明次氯酸是酸,但不能说明次氯酸电离程度,所以不能证明次氯酸是弱酸,故A错误;
B.次氯酸具有强氧化性,具有漂白性,能使品红溶液褪色,该现象体现次氯酸的漂白性,不能说明次氯酸电离程度,所以不能证明次氯酸是弱酸,故B错误;
C.次氯酸见光易分解,说明次氯酸不稳定,但不能说明次氯酸电离程度,所以不能证明次氯酸是弱酸,故C错误;
D.向Ca(ClO)2 溶液中通入CO2能生成次氯酸,碳酸是弱酸,强酸能和弱酸盐反应生成弱酸,说明次氯酸是弱酸,故D正确;
故选D.
点评 本题考查弱电解质判断,为高频考点,强弱电解质的根本区别是电离程度,与电解质稳定性、溶解性无关,易错选项是C.


 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 华北地区水资源十分匮乏,必须节约用水 | |
| B. | 明矾能沉降水中的悬浮物,又能杀菌消毒 | |
| C. | 活性炭既可以吸附水中的异味,又可以降低水的硬度 | |
| D. | 长期饮用纯净水,不利于人体健康 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
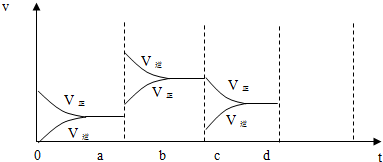
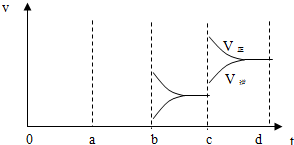 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com