
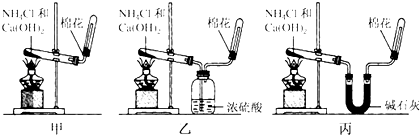
分析 实验室可用氯化铵和氢氧化钙在加热的条件下制备氨气,也可浓氨水与碱石灰制备少量的氨气,氨气的密度比空气小,易溶于水,可用排空法收集,氨气为碱性气体,可与酸反应,检验氨气,可用pH试纸或浓盐酸等,
(1)实验室用氢氧化钙和氯化铵在加热条件下制备氨气;
(2)根据氨气的溶解性和密度选择收集氨气的方法;
(3)氨气能与硫酸反应而被硫酸吸收;
(4)碳酸氢铵加热分解生成氨气、二氧化碳和水,可用碱石灰除杂,但不能用NH4HCO3固体代替NH4Cl固体;
(5)氨气能使湿润的红色石蕊试纸变蓝,所以可以用湿润的红色石蕊试纸检验.
解答 解:实验室可用氯化铵和氢氧化钙在加热的条件下制备氨气,也可浓氨水与碱石灰制备少量的氨气,氨气的密度比空气小,易溶于水,可用排空法收集,氨气为碱性气体,可与酸反应,检验氨气,可用pH试纸或浓盐酸等,
(1)实验室用氢氧化钙和氯化铵在加热条件下制备氨气,反应方程式为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O,
故答案为:2NH4Cl+Ca(OH)2$\frac{\underline{\;\;△\;\;}}{\;}$CaCl2+2NH3↑+2H2O;
(2)氨气易溶于水,不能用排水法收集,氨气密度比空气小,应用向下排空法收集,
故答案为:NH3的密度小于空气;
(3)氨气为碱性气体,通过盛有浓硫酸的洗气瓶时,与硫酸反应而被吸收,
故答案为:乙;
(4)碳酸氢铵加热分解生成氨气、二氧化碳和水,其中可用碱石灰吸收二氧化碳和水,只有丙能做到,
故答案为:丙;
(5)氨气能使湿润的红色石蕊试纸变蓝,所以可以用湿润的红色石蕊试纸检验,检验方法是:将湿润的红色石蕊试纸置于管口,若试纸变蓝,则说明已收集满(或用蘸有浓盐酸的玻璃棒靠近试管口,若有白烟产生,则证明已收集满),
故答案为:将湿润的红色石蕊试纸置于管口,若试纸变蓝,则说明已收集满(或用蘸有浓盐酸的玻璃棒靠近试管口,若有白烟产生,则证明已收集满).
点评 本题考查实验氨气的制取及性质,为高频考点,题目难度中等,明确物质的性质及发生的反应为解答的关键,侧重分析与应用能力的考查,注意氨气的实验室制取方法.


科目:高中化学 来源: 题型:选择题

| A. | a点所示溶液中:c(H2R)+c(HR-)+c(R2-)=0.1mol•L-1 | |
| B. | b点所示溶液中:c(Na+)>c(HR-)>c(H2R)>c(R2-) | |
| C. | c点所示溶液中:c(Na+)<3c(R2-) | |
| D. | d点所示溶液中:c(Na+)>c(R2-)>c(HR-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 25℃时,$\frac{c({H}^{+})}{c(O{H}^{-})}$=1×10-12溶液.Na+、SO32一、ClO-、CO32- | |
| B. | 能与金属铝反应放出氢气的溶液中:K+、Fe2+、Cl-、NO3- | |
| C. | 0.1mol/LBa (OH)2溶液中:Al3+、NH4+、NO3-、HCO3- | |
| D. | 0.1mol/L AlO2-溶液中:Na+、K+、SO32一、CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
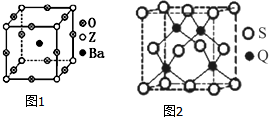 已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素.相关信息如下:
已知X、Y、Z、R、Q为周期表中原子序数依次增大的前36号元素.相关信息如下:| X元素是宇宙中最丰富的元素 |
| Y元素基态原子的核外p电子数比s电子数少1 |
| Z元素被誉为“太空金属”,也有“生物金属”之称,其基态原子次外层有2个未成对电子 |
| R元素在元素周期表的第十一列 |
| Q元素在周期表里与R元素在同一个分区 |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:推断题
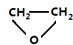 .
.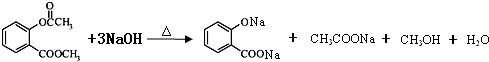 .
.查看答案和解析>>
科目:高中化学 来源: 题型:实验题
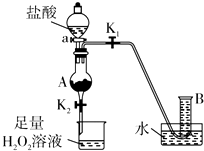 氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如图装置(夹持装置略,气密性已检验):
氯化铁是实验室中的重要试剂.某同学用m g含有铁锈(Fe2O3)的废铁屑来制取FeCl3•6H2O晶体,同时测定废铁屑中铁的质量分数,为此设计了如图装置(夹持装置略,气密性已检验):查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯通入溴水中,测定反应前后溶液pH,pH增大,乙烯与溴发生取代反应 | |
| B. | 向某溶液中加入KSCN溶液和稀盐酸,溶液变红色,原溶液一定有Fe3+ | |
| C. | 将湿润的氨气通过无水CaCl2,可得到干燥的氨气 | |
| D. | 分别取一块小木条,放入饱和硅酸钠溶液和蒸馏水中,充分吸湿、浸透,取出稍沥干后,置于酒精灯外焰处,前者木条未燃烧,后者燃烧,可证明硅酸钠可作木材防火剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
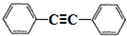 ,以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下:
,以互为同系物的单取代芳烃A、G为原料合成M的一种路线(部分反应条件略去)如下: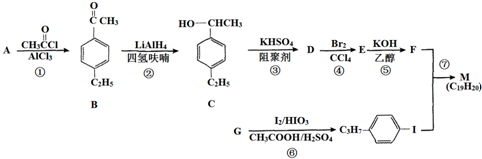
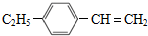 ,分子中最多有10个碳原子共平面,F结构中的官能团名称是碳碳三键;
,分子中最多有10个碳原子共平面,F结构中的官能团名称是碳碳三键;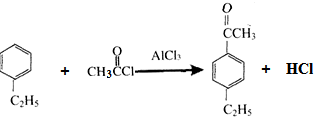 ,④的反应类型是加成反应;
,④的反应类型是加成反应;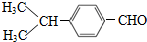 (写结构简式);
(写结构简式);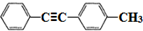 的合成路线
的合成路线 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com