
”¾ĢāÄæ”æŌŚČŻ»żĪŖ1.00LµÄČŻĘ÷ÖŠ£¬ĶØČėŅ»¶ØĮæµÄN2O4£¬·¢Éś·“Ó¦N2O4(g)![]() 2NO2(g) ”÷H£¬ĖęĪĀ¶ČÉżøߣ¬»ģŗĻĘųĢåµÄŃÕÉ«±äÉī”£»Ų“šĻĀĮŠĪŹĢā£ŗ
2NO2(g) ”÷H£¬ĖęĪĀ¶ČÉżøߣ¬»ģŗĻĘųĢåµÄŃÕÉ«±äÉī”£»Ų“šĻĀĮŠĪŹĢā£ŗ
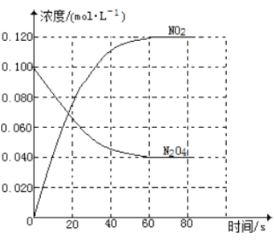
£Ø1£©·“Ó¦µÄ”÷H 0£ØĢī”°£¾”±»ņ”°£¼”±£©£»100”ꏱ£¬ĢåĻµÖŠø÷ĪļÖŹÅضČĖꏱ¼ä±ä»ÆČēĶ¼ĖłŹ¾”£ŌŚ0”«60sŹ±¶Ī£¬·“Ó¦ĖŁĀŹv(NO2)ĪŖ mol”¤L£1”¤s£1£¬·“Ó¦µÄĘ½ŗā³£ŹżKĪŖ ”£
£Ø2£©100”ꏱ“ļĘ½ŗāŗó£¬øı䷓ӦĪĀ¶ČĪŖT£¬c(N2O4)ŅŌ0.0020mol”¤L£1”¤s£1µÄĘ½¾łĖŁĀŹ½µµĶ£¬¾10sÓÖ“ļµ½Ę½ŗā”£ŌņT 100”ę£ØĢī”°“óÓŚ”±»ņ”°Š”ÓŚ”±£©”£
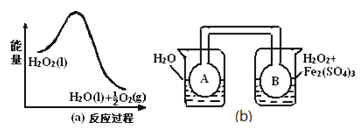
£Ø3£©ĄūÓĆĶ¼£Øa£©ŗĶ£Øb£©ÖŠµÄŠÅĻ¢£¬°“Ķ¼£Øb£©×°ÖĆ£ØĮ¬ĶصÄA”¢BĘæÖŠŅŃ³äÓŠNO2ĘųĢ壩½ųŠŠŹµŃ锣æɹŪ²ģµ½BĘæÖŠĘųĢåŃÕÉ«±ČAĘæÖŠµÄ £ØĢī”°Éī”±»ņ”°Ē³”±£©£¬ĘäŌŅņŹĒ ”£
”¾“š°ø”æ£Ø1£©£¾ 0.0020»ņ2.0”Į10£3 0.36»ņ0.36 mol”¤L£1
£Ø2£©“óÓŚ
£Ø3£©Éī£»N2O4(ĪŽÉ«)![]() 2NO2(ŗģ×ŲÉ«) ”÷H£¾0£¬ŹĒĪüČČ·“Ó¦£¬¶ųĖ«ŃõĖ®µÄ·Ö½ā·“Ó¦ŹĒ·ÅČČ·“Ó¦”£µ±ÓŅ±ßĖ«ŃõĖ®·Ö½āŹ±£¬·Å³öµÄČČĮæ»įŹ¹BĘæÉżĪĀ£¬“Ó¶ųŹ¹ĘæÖŠ·“Ó¦³ÆÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¼“Éś³ÉNO2·½ĻņŅĘ¶Æ£¬¹ŹBĘæŃÕÉ«¼ÓÉī
2NO2(ŗģ×ŲÉ«) ”÷H£¾0£¬ŹĒĪüČČ·“Ó¦£¬¶ųĖ«ŃõĖ®µÄ·Ö½ā·“Ó¦ŹĒ·ÅČČ·“Ó¦”£µ±ÓŅ±ßĖ«ŃõĖ®·Ö½āŹ±£¬·Å³öµÄČČĮæ»įŹ¹BĘæÉżĪĀ£¬“Ó¶ųŹ¹ĘæÖŠ·“Ó¦³ÆÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¼“Éś³ÉNO2·½ĻņŅĘ¶Æ£¬¹ŹBĘæŃÕÉ«¼ÓÉī
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗ£Ø1£©ĖęĪĀ¶ČµÄÉżøߣ¬»ģŗĻĘųĢåµÄŃÕÉ«±äÉī£¬»ÆŃ§Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¼“”÷H£¾0£»0”«60sŹ±¶Ī£¬NO2ÅØ¶Č±ä»ÆĪŖ£ŗ0.12mol/L£¬Ōņv£ØNO2£©=0.12mol/L”Ā60s==0.0020molL-1s-1£»K=c2£ØNO2£©/c£ØN2O4£©=£Ø0.12mol/L£©2/0.04mol/L=0.36mol/L£»
£Ø2£©N2O4µÄÅØ¶Č½µµĶ£¬Ę½ŗāĻņÕż·“Ó¦·½ĻņŅĘ¶Æ£¬ÓÉÓŚÕż·“Ó¦·½ĻņĪüČČ£¬T£¾100”ę£»
£Ø3£©ÓÉÓŚ·“Ó¦N2O4£ØĪŽÉ«£©![]() 2NO2£Øŗģ×ŲÉ«£© ”÷H©0ŹĒĪüČČ·“Ó¦£¬¶ųĖ«ŃõĖ®µÄ·Ö½ā·“Ó¦ŹĒ·ÅČČ·“Ó¦”£µ±ÓŅ±ßĖ«ŃõĖ®·Ö½āŹ±£¬·Å³öµÄČČĮæ»įŹ¹BĘæÉżĪĀ£¬“Ó¶ųŹ¹ĘæÖŠ·“Ó¦³ÆÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¼“ĻņÉś³ÉNO2ŅĘ¶Æ£¬¹ŹBĘæŃÕÉ«øüÉī”£
2NO2£Øŗģ×ŲÉ«£© ”÷H©0ŹĒĪüČČ·“Ó¦£¬¶ųĖ«ŃõĖ®µÄ·Ö½ā·“Ó¦ŹĒ·ÅČČ·“Ó¦”£µ±ÓŅ±ßĖ«ŃõĖ®·Ö½āŹ±£¬·Å³öµÄČČĮæ»įŹ¹BĘæÉżĪĀ£¬“Ó¶ųŹ¹ĘæÖŠ·“Ó¦³ÆÕż·“Ó¦·½ĻņŅĘ¶Æ£¬¼“ĻņÉś³ÉNO2ŅĘ¶Æ£¬¹ŹBĘæŃÕÉ«øüÉī”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠø÷×éĪļÖŹÖŠ£¬Ėłŗ¬·Ö×ÓŹżĻąĶ¬µÄŹĒ
A£®10gH2ŗĶ10gO2 B£®5.6LN2(±ź×¼×“æö)ŗĶ11gCO2
C£® 9gH2OŗĶ1molBr2 D£®224mlH2(±ź×¼×“æö)ŗĶ0.1molN2
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æÓƶčŠŌµē¼«µē½āŅ»¶ØĮæµÄĮņĖįĶČÜŅŗ£¬ŹµŃé×°ÖĆČēĶ¼1ĖłŹ¾£®µē½ā¹ż³ĢÖŠµÄŹµŃ鏿¾ŻČēĶ¼2ĖłŹ¾£¬ŗį×ų±ź±ķŹ¾µē½ā¹ż³ĢÖŠ×ŖŅʵē×ÓµÄĪļÖŹµÄĮæ£¬×Ż×ų±ź±ķŹ¾µē½ā¹ż³ĢÖŠ²śÉśĘųĢåµÄ×ÜĢå»ż£Ø±źæö£©£®ŌņĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ£Ø £©
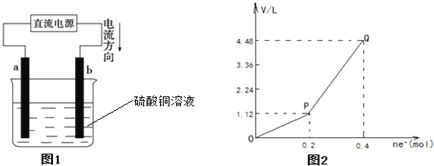
A£®µē½ā¹ż³ĢÖŠ£¬bµē¼«±ķĆęĻČÓŠŗģÉ«ĪļÖŹĪö³ö£¬Č»ŗó²ÅÓŠĘųÅŻ²śÉś
B£®“ÓæŖŹ¼µ½QµćŹ±ŹÕ¼Æµ½µÄ»ģŗĻĘųĢåµÄĘ½¾łĻą¶Ō·Ö×ÓÖŹĮæĪŖ17
C£®ĒśĻßOP¶Ī±ķŹ¾H2ŗĶO2»ģŗĻĘųĢåµÄĢå»ż±ä»Æ£¬ĒśĻßPQ¶Ī±ķŹ¾O2µÄĢå»ż±ä»Æ
D£®aµē¼«ÉĻ·¢Éś·“Ó¦µÄ·½³ĢŹ½ĪŖ£ŗ2H++2e-ØTH2”üŗĶ4OH--4e-ØT2H2O+O2”ü
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”放»Æѧ”Ŗ”ŖŃ”ŠŽ2£ŗ»ÆѧÓė¼¼Źõ”æ
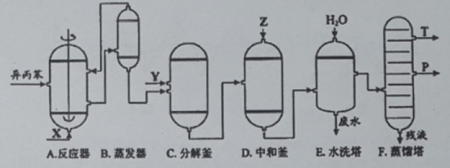
±½·ÓŗĶ±ūĶŖ¶¼ŹĒÖŲŅŖµÄ»Æ¹¤ŌĮĻ£¬¹¤ŅµÉĻæÉÓĆŅģ±ū±½Ńõ»Æ·ØÉś²ś±½·ÓŗĶ±ūĶŖ£¬Ęä·“Ó¦ŗĶ¹¤ŅÕĮ÷³ĢŹ¾ŅāĶ¼ČēĻĀ£ŗ
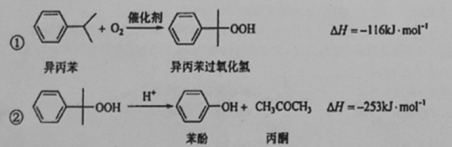
Ļą¹Ų»ÆŗĻĪļµÄĪļĄķ³£Źż
ĪļÖŹ | Ļą¶Ō·Ö×ÓÖŹĮæ | ĆÜ¶Č£Øg/cm£3£© | ·Šµć/”ę |
Ņģ±ū±½ | 120 | 0.8640 | 153 |
±ūĶŖ | 58 | 0.7898 | 56.5 |
±½·Ó | 94 | 1.0722 | 182 |
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©ŌŚ·“Ó¦Ę÷AÖŠĶØČėµÄXŹĒ ”£
£Ø2£©·“Ó¦¢ŁŗĶ¢Ś·Ö±šŌŚ×°ÖĆ ŗĶ ÖŠ½ųŠŠ£ØĢī×°ÖĆ·ūŗÅ£©”£
£Ø3£©ŌŚ·Ö½āøŖCÖŠ¼ÓČėµÄYĪŖÉŁÖĆÅØĮņĖį£¬Ęä×÷ÓĆŹĒ______£¬ÓŵćŹĒÓĆĮæÉŁ£¬Č±µćŹĒ_______________”£
£Ø4£©·“Ó¦¢ŚĪŖ £ØĢī”°·ÅČČ”±»ņ”°ĪüČČ”±£©·“Ó¦”£·“Ó¦ĪĀ¶ČæŲÖĘŌŚ50-60”ę£¬ĪĀ¶Č¹żøߵİ²Č«Ņž»¼ŹĒ ”£
£Ø5£©ÖŠŗĶøŖDÖŠ¼ÓČėµÄZ×īŹŹŅĖµÄŹĒ £ØĢī±ąŗÅ”£ŅŃÖŖ±½·ÓŹĒŅ»ÖÖČõĖį£©”£
a. NaOH b. CaCO3 c. NaHCO3 d. CaO
£Ø6£©ÕōĮóĖžFÖŠµÄĮó³öĪļTŗĶP·Ö±šĪŖ ŗĶ £¬ÅŠ¶ĻµÄŅĄ¾ŻŹĒ ”£
£Ø7£©ÓĆøĆ·½·ØŗĻ³É±½·ÓŗĶ±ūĶŖµÄÓŵćŹĒ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»Æѧ·“Ó¦ÖŠµÄÄÜĮæ±ä»ÆŹĒÓÉ»Æѧ·“Ó¦ÖŠ¾É»Æѧ½”¶ĻĮŃŹ±ĪüŹÕµÄÄÜĮæÓė»Æѧ½”ŠĪ³ÉŹ±·Å³öµÄÄÜĮæ²»Ķ¬ŅżĘšµÄ”£ČēĶ¼ĪŖN2(g)ŗĶO2(g)·“Ӧɜ³ÉNO(g)¹ż³ĢÖŠµÄÄÜĮæ±ä»Æ£¬ĻĀĮŠĖµ·ØÖŠÕżČ·µÄŹĒ
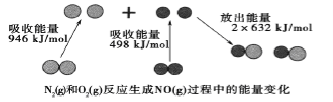
A£®1molN2(g)ŗĶ1molO2(g)·“Ó¦·Å³öµÄÄÜĮæĪŖ180kJ
B£®1molN2(g)ŗĶ1molO2(g)¾ßÓŠµÄ×ÜÄÜĮæŠ”ÓŚ2molNO(g)¾ßÓŠµÄ×ÜÄÜĮæ
C£®ŌŚ1LµÄČŻĘ÷ÖŠ·¢Éś·“Ó¦£®10minÄŚN2¼õÉŁĮĖ1mol£¬Ņņ“Ė10minÄŚµÄĘ½¾ł·“Ó¦ĖŁĀŹĪŖv(NO)=0£®1mol/(L”¤min)
D£®NOŹĒŅ»ÖÖĖįŠŌŃõ»ÆĪļ£¬ÄÜÓėNaOHČÜŅŗ·“Ӧɜ³ÉŃĪŗĶĖ®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠÓŠ¹ŲĻø°ūĪļÖŹ×é³ÉµÄŠšŹö£¬ÕżČ·µÄŹĒ
A. ŌŚČĖĢå»īĻø°ūÖŠĒāŌ×ӵďżÄæ×ī¶ą
B. DNAŗĶRNA·Ö×ӵļī»ł×é³ÉĻąĶ¬
C. ¶ąĢĒŌŚĻø°ūÖŠÖ»ÄÜ×÷ĪŖ“¢ÄÜĪļÖŹ
D. µ°°×ÖŹĒų±šÓŚÖ¬ÖŹµÄĢŲÓŠŌŖĖŲŹĒµŖ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĄė×Ó·½Ź½ŹéŠ“ÕżČ·µÄŹĒ£Ø £©
A£®ŅŃÖŖµēĄėĘ½ŗā³£Źż£ŗH2CO3£¾HClO£¾HCO3-£¬ĻņNaClOČÜŅŗÖŠĶØČėÉŁĮæCO2£ŗ2ClO££«CO2£«H2O£½2HClO£«CO32-
B£®Ļņ·ŠĖ®ÖŠµĪ¼Ó±„ŗĶFeCl3ČÜŅŗÖʱøFe(OH)3½ŗĢå£ŗFe3+£«3H2O = Fe(OH)3”ż£«3H+
C£®Na2SČÜŅŗÖŠµĪ¼ÓNaClOČÜŅŗ£ŗS2£+ClOØC+H2O£½S”ż+Cl£+2OH£
D£®½«ÉŁĮæSO2ĘųĢåĶØČėNaClOČÜŅŗÖŠ£ŗSO2£«H2O£«2ClO£ØTSO32££«2HClO
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”湤ŅµŗĻ³É°±µÄ·“Ó¦ČēĻĀ£ŗN2 + 3H2 ![]() 2NH3”£
2NH3ӣ
ijĪĀ¶ČĻĀ£¬ŌŚČŻ»żŗć¶ØĪŖ2.0LµÄĆܱÕČŻĘ÷ÖŠ³äČė2.0molN2ŗĶ2.0molH2£¬Ņ»¶ĪŹ±¼äŗó·“Ó¦“ļĘ½ŗāדĢ¬£¬ŹµŃ鏿¾ŻČēĻĀ±ķĖłŹ¾£ŗ
t/s | 0 | 50 | 150 | 250 | 350 |
n(NH3) | 0 | 0.24 | 0.36 | 0.40 | 0.40 |
£Ø1£©0~50sÄŚµÄĘ½¾ł·“Ó¦ĖŁĀŹ v(N2) = ”£
£Ø2£©250sŹ±£¬H2µÄ×Ŗ»ÆĀŹĪŖ ”£
£Ø3£©ŅŃÖŖ![]() µÄ¼üÄÜĪŖ946kJ/mol£¬H-HµÄ¼üÄÜĪŖ436kJ/mol£¬N-HµÄ¼üÄÜĪŖ391kJ/mol£¬ŌņÉś³É1molNH3¹ż³ĢÖŠµÄČČĮæ±ä»Æ kJ”£ĻĀĶ¼ÄÜÕżČ·±ķŹ¾øĆ·“Ó¦ÖŠÄÜĮæ±ä»ÆµÄŹĒ________”£
µÄ¼üÄÜĪŖ946kJ/mol£¬H-HµÄ¼üÄÜĪŖ436kJ/mol£¬N-HµÄ¼üÄÜĪŖ391kJ/mol£¬ŌņÉś³É1molNH3¹ż³ĢÖŠµÄČČĮæ±ä»Æ kJ”£ĻĀĶ¼ÄÜÕżČ·±ķŹ¾øĆ·“Ó¦ÖŠÄÜĮæ±ä»ÆµÄŹĒ________”£

£Ø4£©ĪŖ¼Óæģ·“Ó¦ĖŁĀŹ£¬æÉŅŌ²ÉČ”µÄ“ėŹ©
a£®½µµĶĪĀ¶Č
b£®Ōö“óŃ¹Ēæ
c£®ŗćČŻŹ±³äČėHeĘų
d£®ŗćŃ¹Ź±³äČėHeĘų
e£®¼°Ź±·ÖĄėNH3
£Ø5£©ĻĀĮŠĖµ·Ø“ķĪóµÄŹĒ
A£®Ź¹ÓĆ“ß»Æ¼ĮŹĒĪŖĮĖ¼Óæģ·“Ó¦ĖŁĀŹ£¬ĢįøßÉś²śŠ§ĀŹ
B£®ÉĻŹöĢõ¼žĻĀ£¬N2²»æÉÄÜ100%×Ŗ»ÆĪŖNH3
C£®ĪŖĮĖĢįøßN2µÄ×Ŗ»ÆĀŹ£¬Ó¦ŹŹµ±ĢįøßH2µÄÅضČ
D£®250~350sÉś³ÉĪļÅØ¶Č±£³Ö²»±ä£¬·“Ó¦Ķ£Ö¹
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĶ¼1ŹĒĶŠæŌµē³ŲŹ¾ŅāĶ¼”£Ķ¼2ÖŠxÖį±ķŹ¾ŹµŃ鏱Į÷ČėÕż¼«µÄµē×ÓµÄĪļÖŹµÄĮ棬yÖį±ķŹ¾( )
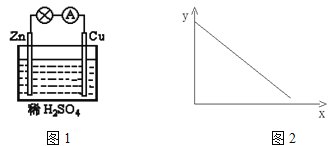
A£®Ķ°ōµÄÖŹĮæ B£®c(Zn2+) C£®c(H+) D£®c(SO42-)
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com