
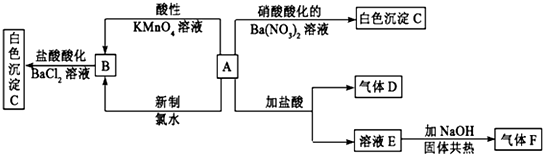
分析 A为含硫氮正盐其中硫元素化合价为+4,与盐酸反应生成气体D与气体F,而气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝,则D为SO2,F为NH3,A是(NH4)2SO3,E为NH4Cl,故白色沉淀C为BaSO4,B为(NH4)2SO4.
解答 解:A为含硫氮正盐其中硫元素化合价为+4,与盐酸反应生成气体D与气体F,而气体D能使品红溶液褪色,气体F能使湿润的红色石蕊试纸变蓝,则D为SO2,F为NH3,A是(NH4)2SO3,E为NH4Cl,故白色沉淀C为BaSO4,B为(NH4)2SO4.
(1)由上述分析,D为SO2,F为NH3,
故答案为:SO2;NH3;
(2)①A和酸性KMnO4溶液反应离子方程式为:2MnO4-+6H++5SO32-=5SO42-+2Mn2++5H2O,
②D和新制氯水反应离子方程式为:SO2+Cl2+2H2O=SO42-+4H++2Cl-,
故答案为:2MnO4-+6H++5SO32-=5SO42-+2Mn2++5H2O;SO2+Cl2+2H2O=SO42-+4H++2Cl-;
(3)硝酸具有强氧化性,可以将SO32-氧化为SO42-,会影响SO42-的检验,在检验SO42-时,应使用 盐酸酸化的BaCl2溶液,
故选:A.
点评 本题考查无机物的推断,D、F的性质是推断突破口,熟练掌握元素化合物性质,注意掌握常见离子检验.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 用CCl4鉴别溴水和碘水 | |
| B. | 用AgNO3溶液鉴别溴化钾溶液和氯化钠溶液 | |
| C. | 向某盐溶液中加入氢氧化钠溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,溶液中一定有NH4+ | |
| D. | 向某盐溶液中,加入盐酸,产生使澄清石灰水变浑浊的气体,溶液中含有大量CO32-离子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温下,4体积pH=9的Ca(OH)2溶液与1体积pH=13的NaOH溶液混合后,氢离子浓度是1×10-13mol/L | |
| B. | 用盐酸滴定氨水时,能用酚酞做指示剂(酚酞的变色范围是pH=8~10) | |
| C. | 加热Na2CO3溶液、NaHCO3溶液和CO2与H2O饱和溶液,它们的pH值都会上升 | |
| D. | pH相同的氨水、氢氧化钠用蒸馏水稀释到原来的x倍、y倍至pH仍相同,则x<y |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲烷的标准燃烧热为-890.3 kJ•mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)═CO2(g)+2H2O (g)△H=-890.3 kJ•mol-1 | |
| B. | 相同条件下,2mol氢原子所具有的能量小于1mol氢分子所具有的能量 | |
| C. | 常温下,反应C(s)+CO2(g)═2CO(g) 不能自发进行,则该反应的△H<0 | |
| D. | 已知①2H2(g)+O2(g)═2H2O (g)△H1=a kJ•mol-1②2H2(g)+O2(g)═2H2O (l)△H2=b kJ•mol-1,则a>b |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com