
| ||
| △ |
| ||
| △ |
| ||
| (10-9.38)g×168g |
| 62g |
| 8.32g |
| 10g |
| ||
| ||


 字词句篇与同步作文达标系列答案
字词句篇与同步作文达标系列答案科目:高中化学 来源: 题型:
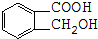 .试回答:
.试回答:查看答案和解析>>
科目:高中化学 来源: 题型:
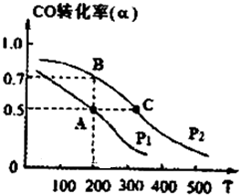 工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:
工业上一般以CO和H2为原料合成甲醇,该反应的热化学方程式为:| 1 |
| 2 |
| C(H2) |
| C(CH3OH) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | ||
| M |
查看答案和解析>>
科目:高中化学 来源: 题型:
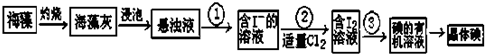
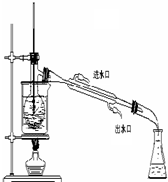
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HNO3在反应中既表现氧化性也表现出酸性 |
| B、每生成22.4L NO(标准状况)有3mol电子转移 |
| C、HNO3作氧化剂,铜作还原剂,3mol Cu还原8mol的HNO3 |
| D、HNO3作氧化剂,铜作还原剂,3mol Cu还原2mol的HNO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、原子半径:X>Y>Q>W |
| B、元素Y与元素Z的最高正化合价之和的数值等于8 |
| C、Q和Z所形成的化合物为共价化合物 |
| D、X、Q和W三种元素形成的化合物的水溶液呈碱性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、HCl |
| B、少量Na2SO3 |
| C、少量NaOH |
| D、CaCO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com