
【题目】草酸是植物(特别是草本植物)常具有的成分,具有广泛的用途。草酸晶体(H2C2O4·2H2O)无色,熔点为101℃,易溶于水,受热易脱水、升华,170℃以上分解。常温下它的电离常数K1=5.4×10-2,K2=5.4×10-5。回答下列问题:
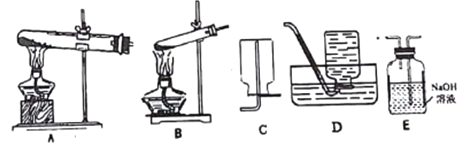
I.拟用下列装置分解草酸制备少量纯净的CO,其合理的连接顺序为________(填字母序号)。
Ⅱ.设计实验证明草酸为弱酸的方案及其现象均正确的有______(填序号)。
A.室温下,取0.010mol/L的H2C2O4溶液,测其pH=2;
B.室温下,取0.010mol/L的NaHC2O4溶液,测其pH>7;
C. 室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后,测其pH
D.标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL
Ⅲ.医学上常用酸性KMnO4溶液和草酸(H2C2O4)溶液反应来测血液中血钙的含量。测定方法是:取2mL血液用蒸馏水稀释后.向其中加入足量的(NH4)2C2O4溶液,反应生成CaC2O4沉淀,将沉淀用稀硫酸溶解得到H2C2O4后,再用KMnO4溶液滴定。
①溶解沉淀时______(填“能”或“不能”)用稀盐酸,原因是_________。
②滴定时,用______(填“酸”或“碱”)式滴定管装KMnO4溶液,滴定达到终点的现象是______。
③ 滴定过程中发生的离子反应方程式______________。
④ 若上述滴定中消耗了1.0×10-4mol/LKMnO4的溶液20mL,则200mL该血液中含钙_____g。
⑤ 下列操作会引起测定结果偏高的是__________(填序号)
A.滴定管在盛装KMnO4溶液前未润洗
B.滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出
C.滴定前读数正确,滴定终点时俯视读数
D.装待测液的锥形瓶用蒸馏水洗涤后,没用待测液冲洗
【答案】 BED C 不能 KMnO4也能氧化盐酸 酸 当加入最后一滴KMnO4,溶液变为紫红色且30s不变 2MnO4-+5H2C2O4+6H+=2Mn2++10CO2 +8H2O 0.02 A
【解析】试题分析:本题考查气体制备实验装置的连接,氧化还原滴定实验和误差分析,实验方案的设计和评价。
I.草酸晶体的熔点为101℃低于其分解温度170℃,所以气体发生装置选B;草酸晶体分解的方程式为H2C2O4·2H2O![]() CO↑+CO2↑+3H2O,分解得到的CO中混有CO2,要将混合气通过NaOH溶液除去CO2;由于CO的密度与空气相近,CO难溶于水,所以用排水法收集CO;装置的合理连接顺序为BED。
CO↑+CO2↑+3H2O,分解得到的CO中混有CO2,要将混合气通过NaOH溶液除去CO2;由于CO的密度与空气相近,CO难溶于水,所以用排水法收集CO;装置的合理连接顺序为BED。
II.A项,草酸是二元弱酸,室温下0.010mol/L的H2C2O4溶液的pH![]() 2,现象不正确;B项,常温下草酸的电离常数K1=5.4×10-2、K2=5.4×10-5,HC2O4-水解方程式为HC2O4-+H2O
2,现象不正确;B项,常温下草酸的电离常数K1=5.4×10-2、K2=5.4×10-5,HC2O4-水解方程式为HC2O4-+H2O![]() H2C2O4+OH-,HC2O4-的水解常数为KW/K1=1
H2C2O4+OH-,HC2O4-的水解常数为KW/K1=1![]() 10-14
10-14![]() (5.4×10-2)=1.85
(5.4×10-2)=1.85![]() 10-13
10-13![]() 5.4
5.4![]() 10-5,HC2O4-的电离程度大于HC2O4-的水解程度,室温下0.010mol/L的NaHC2O4溶液的pH
10-5,HC2O4-的电离程度大于HC2O4-的水解程度,室温下0.010mol/L的NaHC2O4溶液的pH![]() 7,现象不正确;C项,室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后测其pH<a+2,说明加水稀释过程中H2C2O4继续电离产生H+,能说明草酸是弱酸;D项,标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL只能说明草酸是二元酸,不能说明草酸是弱酸;答案选C。
7,现象不正确;C项,室温下,取pH=a(a<3)的H2C2O4溶液稀释100倍后测其pH<a+2,说明加水稀释过程中H2C2O4继续电离产生H+,能说明草酸是弱酸;D项,标况下,取0.10mol/L的H2C2O4溶液100mL与足量锌粉反应,收集到H2体积为224mL只能说明草酸是二元酸,不能说明草酸是弱酸;答案选C。
III. ①溶解沉淀时不能用稀盐酸,原因是KMnO4也能氧化盐酸,反应的离子方程式为2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O。
②滴定时,用酸式滴定管装KMnO4溶液,因为KMnO4具有强氧化性,会腐蚀碱式滴定管的橡皮管,所以不能用碱式滴定管。滴定达到终点的现象是当加入最后一滴KMnO4,溶液变为紫红色且30s不变。
③滴定过程中KMnO4将H2C2O4氧化成CO2,发生的离子反应方程式为2MnO4-+5H2C2O4+6H+=2Mn2++10CO2 ↑+8H2O。
④若上述滴定中消耗了1.0×10-4mol/LKMnO4的溶液20mL,根据关系式5Ca2+~5CaC2O4~5H2C2O4~2KMnO4,n(Ca)=5/2c(KMnO4)V[KMnO4(aq)]=5/2![]() 1.0
1.0![]() 10-4mol/L
10-4mol/L![]() 0.02L=5
0.02L=5![]() 10-6mol,200mL该血液中含钙5
10-6mol,200mL该血液中含钙5![]() 10-6mol
10-6mol ![]() 40g/mol
40g/mol![]() =0.02g。
=0.02g。
⑤A项,滴定管在盛装KMnO4溶液前未润洗,所耗KMnO4溶液体积偏高,测定结果偏高;B项,滴定过程中,锥形瓶振荡的太剧烈,以致部分液体溅出,所耗KMnO4溶液体积偏低,测定结果偏低;C项,滴定前读数正确,滴定终点时俯视读数,所耗KMnO4溶液体积偏低,测定结果偏低;D项,装待测液的锥形瓶用蒸馏水洗涤后,没用待测液冲洗,所耗KMnO4溶液体积偏低,测定结果偏低;引起测定结果偏高的是A,答案选A。


 愉快的寒假南京出版社系列答案
愉快的寒假南京出版社系列答案科目:高中化学 来源: 题型:
【题目】2018年10月3日瑞典皇家科学院宣布,将授予美国科学家弗朗西斯·阿诺德(FrancesH.Arnold)、美国科学家乔治·史密斯(GeorgeP.Smith)及英国科学家格雷戈里· 温特尔(Sir GregoryP.Winter)三位科学家2018诺贝尔化学奖,以表彰他们在酶的定向演化以及用于多肽和抗体的噬菌体展示技术方面取得的成果。在物质的分类上,酶属于
A. 单质 B. 无机物 C. 有机物 D. 氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知反应4NH3+5O2=4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)(mol·L-1·min-1)表示,则下列关系正确的是( )
A. 4v(NH3)=5v(O2) B. 6v(O2)=5v(H2O) C. 2v(NH3)=3v(H2O) D. 5v(O2)=4v(NO)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用图所示装置进行下列实验:将①中溶液滴入②中,预测的现象与实际相符的是 ( ) 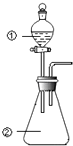
选项 | ①中物质 | ②中物质 | 预测②中的现象 |
A | 稀硫酸 | 硝酸亚铁溶液 | 无明显现象 |
B | 浓硝酸 | 用砂纸打磨过的铝条 | 产生红棕色气体 |
C | 氯化铝溶液 | 浓氢氧化钠溶液 | 立即产生大量白色沉淀 |
D | 草酸溶液 | 高锰酸钾酸性溶液 | 溶液逐渐褪色 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关氯水的叙述,正确的是( )
A.新制氯水中只含有氯气和次氯酸分子
B.新制氯水可使紫色石蕊试液先变红后褪色
C.氯水光照时有气泡逸出,该气体的主要成分是氯气
D.氯水放置数天后,其导电能力减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列操作会促进水的电离,且使溶液pH>7的是( )
A.将纯水加热到90 ℃ B.向水中加入少量NaOH
C.向水中加入少量Na2CO3 D.向水中加入少量FeCl3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质的工业制法正确的是
A.制钛:用金属钠置换出氯化钛(TiCl4)溶液中的钛
B.炼铁:炼铁高炉中碳在高温下还原铁矿石中的铁
C.制钠:用海水作原料制得精盐,再电解熔融的氯化钠得到金属钠
D.炼硅:用焦炭与二氧化硅在高温下反应生成粗硅和二氧化碳
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镁及其合金广泛应用于航空航天、交通、电池等行业。
已知:CaO(s)+3C(s)=CaC2(s)+CO(g) △H= +464 kJ·mol-1
MgO(s)+ CaC2(s)=CaO(s)+ Mg(g)+2C(s) △H =+177.5 kJ·mol-1
(1)镁可以在二氧化碳中燃烧,写出化学反应方程式_____________________。
(2)写出MgO(s)与C(s)生成1 mol CO(g)和气态镁的热化学方程式:________________。
(3) 用电解法制取镁时,若原料氯化镁含有水时,在电解温度下,原料会形成Mg(OH)Cl,并发生电离反应:Mg(OH)Cl=Mg(OH)++Cl-。电解时在阴极表面会产生氧化镁钝化膜,此时阴极的反应式为________________。
(4)镁/间二硝基苯电池工作时镁转变为氢氧化镁,间二硝基苯则转变为间二苯胺。间二硝基苯、间二苯胺的结构简式和镁/间二硝基苯电池的装置如下:
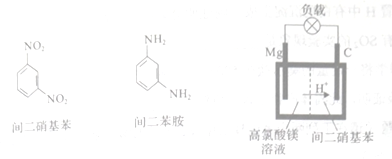
该电池放电时的正极反应方程式为___________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com