
����Ŀ����1��ij����С���о��������������������£��ı���ʼ�������ʵ�������n��H2����ʾ����N2(g)��3H2(g) ![]() 2NH3(g) ��H < 0��Ӧ��Ӱ�죬ʵ�����ɱ�ʾ������ͼ��ʾ�Ĺ��ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�������
2NH3(g) ��H < 0��Ӧ��Ӱ�죬ʵ�����ɱ�ʾ������ͼ��ʾ�Ĺ��ɣ�ͼ��T��ʾ�¶ȣ�n��ʾ���ʵ�������
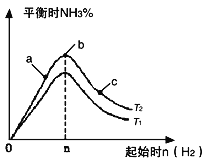
�� �Ƚ���a��b��c����������ƽ��״̬�У���Ӧ��N2��ת������ߵ���_____________��
�� �������ݻ�Ϊ1L��n��3mol����Ӧ�ﵽƽ��ʱH2��ת����Ϊ60%��H2�� N2���ʵ���֮��Ϊ3��1��������ʼʱ��ϵ�м���N2�����ʵ���Ϊ___________mol���������£�T2������Ӧ��ƽ�ⳣ��K �� ______________��
�� ͼ����T2��T1�Ĺ�ϵ��T2_____________ T1������ڡ��������ڡ��������ڡ�������ȷ��������
��2��N2O5��һ����������������һ���¶��¿ɷ������·�Ӧ��2 N2O5 (g)4NO2(g)+O2(g)��H��0T1�¶�ʱ�����ܱ�������ͨ��N2O5������ʵ�����ݼ��±���
ʱ��/s | 0 | 500 | 1000 | 1500 |
c(N2O5)/molL-1 | 5.00 | 3.52 | 2.50 | 2.50 |
�ٴ�ƽ��������������䣬�����������ѹ����ԭ����![]() ����c��N2O5��_______������ڡ�����С�ڡ��������ڡ�������ȷ������5.00molL-1
����c��N2O5��_______������ڡ�����С�ڡ��������ڡ�������ȷ������5.00molL-1
��500s��N2O5�ֽ�����Ϊ ____________��
��T1�¶��� ƽ��ʱN2O5��ת����Ϊ____________��
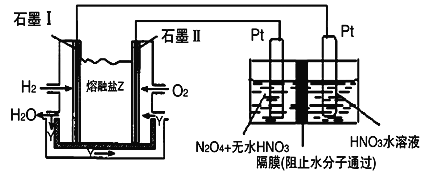
��3������H2��O2��������Na2CO3��ɵ�ȼ�ϵ�أ���ͼ��ʾ������YΪCO2��װ�ý��е�⡣
д��ʯīII�缫�Ϸ�����Ӧ�ĵ缫��Ӧʽ__________________ ��
�ڵ���������N2O5�ĵ缫��ӦʽΪ__________________ ��
���𰸡� �������1��c �������2��n��3(��1mol) �������3��K��25��12��2.08 �������4������ �������5������ �������6��2.96��10-3molL-1s-1 �������7��50% �������8��O2��4e����2CO2 �� 2 CO32�� �������9��������N2O4��2HNO3 �� e�� �� 2N2O5 + 2H��
����������1�����⿼�黯ѧƽ�ⳣ����Ӱ�컯ѧƽ���ƶ������أ���x����������������������������������˷�Ӧ���Ũ�ȣ�ƽ��������Ӧ�����ƶ�����N2��ת�����������N2��ת������ߵ���c�����ʼʱͨ��N2����Ϊxmol��
N2(g)��3H2(g) ![]() 2NH3(g)
2NH3(g)
��ʼ�� x 3 0
�仯�� 60% 3��60% 1.2
ƽ�⣺x��0.6 1.2 1.2 �ﵽƽ�������͵��������ʵ���֮��Ϊ3��1����1.2��(x��0.6)=3��1�����x=1������Ϊ1L�����ݻ�ѧƽ�ⳣ���Ķ��壬K=c2(NH3)//[c3(H2)��c(N2)]=1.22/(1.23��0.4)=25/12���۴˷�Ӧ�Ƿ��ȷ�Ӧ�������¶ȣ�ƽ�����淴Ӧ������У�NH3�����������С�����T1>T2����2�����⿼�黯ѧƽ����㡢��ѧ��Ӧ���ʵļ��㣬�����������ѹ��Ϊԭ����1/2������ƽ�ⲻ�ƶ�����ʱc(N2O5)=5mol��L��1����Ӧǰ����ϵ��֮��С�ڷ�Ӧ������ϵ��֮�ͣ��������ѹǿ��ƽ�����淴Ӧ������У�c(N2O5)>5mol��L��1���ڸ��ݻ�ѧ��Ӧ���ʵ���ѧ����ʽ��v(N2O5)=(5��3.52)/500mol/(L��s)=2.96��10��3 mol/(L��s)����1000sʱ�ﵽƽ�⣬N2O5��ת����Ϊ(5��2.5)/5��100%=50%����3�����⿼��ȼ�ϵ�ص缫��Ӧʽ��д�Լ������е缫��Ӧʽ����д��ʯīIIͨ����������ʯīIIΪ������������������Σ�����ȼ�ϵ�ص�װ��ͼ��������ͨ�������Ͷ�����̼�����������ӦʽΪCO2��CO32����4e��=2CO32�������ݵ��ص�װ��ͼ�����Pt���ӵ�ص��������Ҷ�Pt���ӵ�صĸ�������N2O4��N2O5�����ϼ����ߣ�ʧ���ӣ����N2O5�������ϲ�����������˲������缫��ӦʽΪN2O4��2HNO3��e��=2N2O5��2H����


 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������������ԭ�����͵���
����ѩ�̵�ƿ�ǣ������������ݳ�
����H2��I2��HI����������ɵ�ƽ����ϵ��ѹ����ɫ����
������Ũ��ˮ���������ƹ������������ư�
�����շ����������������SO2����
��ʹ������ý��ʹN2��H2�Ļ�����������ںϳ�NH3
������������еİ���Һ�������ںϳɰ���Ӧ
��500�����ұ����¸������ںϳ�NH3
������FeCl2��Һʱ����������м
��ʵ���ҳ����ű��ͺ�ʳ��ˮ���ռ�Cl2
A. 3�� B. 4�� C. 5�� D. 6��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ӧ4NH3 (g) +5O2(g)![]() 4NO(g) +6H2O(g)�� ��H=-a kJmol-1����5L�ܱ�����Ͷ��1molNH3��1mol��O2��2���Ӻ�NO�����ʵ���������0.4mol������˵����ȷ����
4NO(g) +6H2O(g)�� ��H=-a kJmol-1����5L�ܱ�����Ͷ��1molNH3��1mol��O2��2���Ӻ�NO�����ʵ���������0.4mol������˵����ȷ����
A. 2���ӷ�Ӧ�ų�����.��ֵС��0.1akJ
B. ��������ʾ2���ӵķ�Ӧ���ʣ�v(O2)=0.05mol ��L-1 ��min-1
C. 2������NH3��ת������50��
D. 2����ĩ c(H2O)=0.6mol/L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����һ��ȼ�ϵ�أ�����ȼ��ΪH2�Ϳ����������Ϊ���ڵ�K2CO3���ش���������
��CO![]() ����____________����
����____________����
��������ӦʽΪ____________________��
�۵����CO![]() �����ʵ�������________________���������١����䣩��
�����ʵ�������________________���������١����䣩��
��2��������ĵ�ض������ʽ��е�⣬����a��b��c��d��e��f�缫��Ϊ���Ե缫��ͨ���a���������������Զ���b����2���Ӻ���ҳص�pHΪ12����
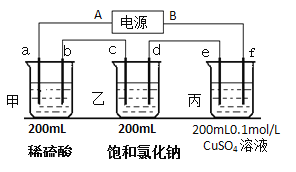
�ٵ�ԴA����______________����
��c���ϵĵ缫��Ӧʽ��___________________��
�ۼס������ع����ռ���________mol���塣
�ܱ�װ����ij������������________�ˣ���Һ��pHΪ________________�������£���������Һ����仯��
�ݵ��n���Ӻ�����ͭ���������꣬�ٽ�e��f�缫���ӵ�Դ����ͬ���ĵ����ٵ��n���ӣ������Һ�е�����ͭ�����ʵ���Ũ��Ϊ______________mol/L������������Һ����仯��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A�� N2��Ħ������Ϊ18g B�������ʵ�����O2��O3����������ԭ������ͬ
C�� 44g CO2�����Ϊ22.4L D��4.9 g H2SO4����0.05NA��H2SO4����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������в����ڸ߷��ӻ��������
A. ������ B. �Ҵ� C. ���� D. ����ϩ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧʽ��ֻ�ܱ�ʾһ�����ʵ���(����)
A. C3H7OH B. CH2O C. C2H6O D. C3H6O2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й����ʵ���������;���ж�Ӧ��ϵ���ǣ�������
A.SO2���������ԣ�������Ư��ֽ��
B.NH4HCO3�����ֽ⣬����������
C.Fe2��SO4��3������ˮ����������ˮ��
D.Al2O3�۵�ߣ����������²���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com