
分析 C原子最外层电子数是E原子最外层电子数的3倍,设E的最外层电子数为x,则C的最外层电子数为3x,因为B、C、E原子的最外层电子数之和为13,若X=1,则B的最外层电子数为9,不符合实际,若x=3,则C的最外层电子数为9,也不符合实际,所以x只能等于2,此时,C的最外层电子数为6,B的最外层电子数为5,B、F原子最外层电子数之和等于C、E原子最外层电子数之和,则F的最外层电子数为3,由于短周期主族元素A、B、C、D、E、F的原子序数依次递增,所以E、F只能在第三周期,E为镁元素,F为铝元素,B、C在第二周期,B为氮元素,C为氧元素,元素C和D可形成两种化合物D2C、D2C2,则D为钠元素,A、B两元素相邻,所以A为碳元素,据此答题
解答 解:C原子最外层电子数是E原子最外层电子数的3倍,设E的最外层电子数为x,则C的最外层电子数为3x,因为B、C、E原子的最外层电子数之和为13,若X=1,则B的最外层电子数为9,不符合实际,若x=3,则C的最外层电子数为9,也不符合实际,所以x只能等于2,此时,C的最外层电子数为6,B的最外层电子数为5,B、F原子最外层电子数之和等于C、E原子最外层电子数之和,则F的最外层电子数为3,由于短周期主族元素A、B、C、D、E、F的原子序数依次递增,所以E、F只能在第三周期,E为镁元素,F为铝元素,B、C在第二周期,B为氮元素,C为氧元素,元素C和D可形成化合物D2C2,则D为钠元素,A、B两元素相邻,所以A为碳元素.
(1)E为镁元素,在元素周期表的第三周期IIA族,故答案为:Mg;三;IIA;
(2)元素A、B形成的最简单的气态氢化物稳定性强弱关系为NH3>CH4,元素C和D可形成D2C2,为过氧化钠,含有的离子键、非极性共价键,故答案为:NH3>CH4,离子键、非极性共价键;
(3)铝和氢氧化钠溶液发生反应的离子方程式为2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑,氢气与氧气构成的燃料电池,在30%KOH溶液为电解质溶液的这种电池的负极反应式为:H2-2e-+2OH-=2H2O,故答案为:2Al+2OH-+6H2O═2[Al(OH)4]-+3H2↑,H2-2e-+2OH-=2H2O;
(4)NH3的水溶液可作刻蚀剂H2O2的清除剂,所发生反应的产物不污染环境,反应生成氮气与水,化学方程式为:2NH3•H2O+3H2O2=N2↑+8H2O,故答案为:2NH3•H2O+3H2O2=N2↑+8H2O.
点评 本题主要考查了元素周期表、元素周期律、元素化合物知识、离子反应等知识,中等难度,解题的难点在于元素的推断.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:实验题
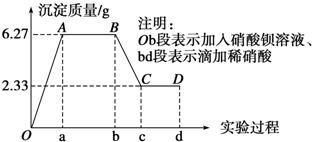
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 由H形成1 mol H-H键要吸收热量 | |
| B. | 所有燃烧反应都是放热反应 | |
| C. | 16g O3单质中含有的分子个数为NA | |
| D. | 凡经加热而发生的化学反应都是吸热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe与稀硝酸、稀硫酸反应均产生气泡,说明Fe与两种酸均发生置换反应 | |
| B. | 向AlCl3溶液中滴加氨水,产生白色沉淀;再加入过量NaHSO4溶液,沉淀消失 | |
| C. | Fe(OH)3胶体无色、透明,能发生丁达尔效应 | |
| D. | SiO2既能和NaOH溶液反应,又能和氢氟酸反应,所以SiO2是两性氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
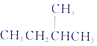 ④
④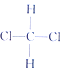 和
和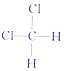 ⑤CH3CH2CH2CH3和
⑤CH3CH2CH2CH3和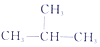
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
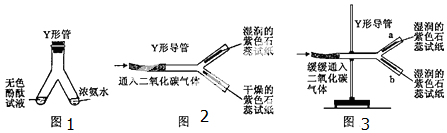
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 12C与14C互称同位素,O2与O3是氧元素的同素异形体 | |
| B. | SO2和SO3属于酸性氧化物,Na2O和Na2O2属于碱性氧化物 | |
| C. | 潮解和电解属于化学变化,蒸馏和干馏属于物理变化 | |
| D. | 沼气和水煤气属于可再生能源,锌锰干电池和铅蓄电池属于二次电池 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com