
| 催化剂 |
| 投料比[n(H2)/n(CO2)] | 500K | 600K | 700K | 800K |
| 1.5 | 45% | 33% | 20% | 12% |
| 2.0 | 60% | 43% | 28% | 15% |
| 3.0 | 83% | 62% | 37% | 22% |


科目:高中化学 来源: 题型:
| A、①②③④ | B、④①②③ |
| C、①④②③ | D、①④③② |
查看答案和解析>>
科目:高中化学 来源: 题型:
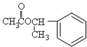
| A、该栀子酯的分子式C10H11O2 |
| B、栀子酯的一氯代物有六种 |
| C、栀子酯可以发生加成、取代和消去反应 |
| D、1mol栀子酯水解需要消耗2molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.0 mol?L-1 KNO3溶液:H+、Fe2+、SCN-、SO42- | ||
B、
| ||
| C、由水电离产生c (H+)=10-10mol/L的溶液:NH4+、AlO2-、Ca2+、S2- | ||
| D、c(ClO-)=1.0 mol?L-1的溶液:K+、SO32-、S2-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
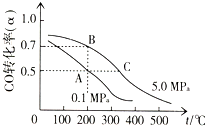 科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,产出了高热值的煤炭气,主要成分是CO和H2.
科研人员通过向地下煤层气化炉中交替鼓入空气和水蒸气的方法,产出了高热值的煤炭气,主要成分是CO和H2.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、室温下反应C(s)+CO2(g)=2CO(g)不能自发进行,说明其△H<0 |
| B、25℃时PH=5的盐酸和PH=9的氨水,两溶液中水的电离程度不同 |
| C、25℃时Ksp(A)>Ksp(B),说明化合物A的溶解度比化合物B的大 |
| D、在NH4Cl溶液中加入适量的硫酸,可使c(NH4+):c(Cl-)接近1:1 |
查看答案和解析>>
科目:高中化学 来源: 题型:
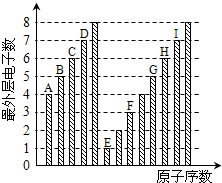
| A、原子半径:A<B<C<D |
| B、E和C元素形成的化合物中只可能存在离子键 |
| C、气态氢化物稳定性:I>D>H>G |
| D、E、F和H三种元素相应的最高价氧化物对应水化物之间两两会发生反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、0.1mol/L稀盐酸中,Cl-数为0.1NA |
| B、2.24 L NH3中含N-H键数目为0.3NA |
| C、2.8g N2和2.8g CO所含分子数均为0.1NA |
| D、0.lmol H2O2完全分解转移的电子数为0.2NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com