
| 3.584L |
| 22.4L/mol |
| 3.584L |
| 22.4L/mol |
| 0.7mol-0.16mol |
| 2 |
| 0.02mol×89g/mol |
| 0.02mol×89g/mol+16.020g |


 金牌课堂练系列答案
金牌课堂练系列答案 三新快车金牌周周练系列答案
三新快车金牌周周练系列答案科目:高中化学 来源: 题型:
| A、食盐是常用的调味剂和防腐剂 |
| B、淀粉在人体中最终水解为葡萄糖而被吸收 |
| C、多吃含钙丰富的豆腐可预防骨质疏松 |
| D、多吃富含维生素A的鱼肝油可预防坏血病 |
查看答案和解析>>
科目:高中化学 来源: 题型:


查看答案和解析>>
科目:高中化学 来源: 题型:
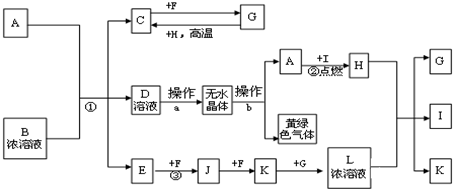
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 主族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 二 | ① | ② | ||||||
| 三 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
| 四 | ⑨ | ⑩ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、铁是较活泼的金属,它与卤素(X2)反应的生成物均为FeX3 |
| B、氢氧化铁可以由相应的物质通过化合反应而制得 |
| C、氢氧化铁与氢碘酸反应:Fe(OH)3+3HI═FeI3+3H2O |
| D、铁元素位于周期表中第4周期第VIIIB族 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com