

���� ��ͭ����������ͭ��Ҫ��������ͭ���轫����ȥ����˿ɼ�������ϡ���Ὣ����ȥ��XΪϡ���ᣬͭ�������Ӧ�����˺�ͭ��������Ӧת��Ϊ����ͭ������ͭ�����ᷴӦ��������ͭ��
��1������������֪XΪ�ܽ�����ͭ������Լ�Ϊϡ���
��2��ͭ��Ũ������ȷ�Ӧ��������ͭ�����������ˮ��
��3��;������ͭ��Ũ���ᷴӦ��������ͭ�����������ˮ����˶Ա�;��I����;����û�ж����������������Ⱦ��
a��;����IJ��������;����࣬����������Ⱦ��
b��;�������;�����ʡԭ�ϣ��Ҳ�������Ⱦ
c��ͭԪ���غ��������
d��ÿ����1molBΪ����ͭ����ͭ��������Ӧ��������ͭ������0.5mol��������ת��2mol���ӣ�
��4��25g�������ʵ���=$\frac{25g}{250g/mol}$=0.1mol��������ȴ��������������������7.2g���ʵ���=$\frac{7.2g}{18g/mol}$=0.4mol�����CuSO4•5H2O��֪ʧȥ�Ľᾧˮ���õ�����Ļ�ѧʽ��
��� �⣺��ͭ����������ͭ��Ҫ��������ͭ���轫����ȥ��XΪϡ���ᣬ��˿ɼ�������ϡ���Ὣ����ȥ��ͭ�������Ӧ�����˺�ͭ��������Ӧת��Ϊ����ͭ������ͭ�����ᷴӦ��������ͭ��Һ������Ũ������ȴ�ᾧ������ϴ�ӵõ�����ͭ���壬;������ͭ��Ũ������ȷ�Ӧ��������ͭ��Һ��������ͬʱ������Ⱦ�������������
��1������������֪�õ�XΪϡ���ᣬ�ʴ�Ϊ��ϡ���
��2��;������ͭ��Ũ���ᷴӦ��������ͭ�����������ˮ����Ӧ�Ļ�ѧ����ʽΪCu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O��
�ʴ�Ϊ��Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O��
��3��;������ͭ��Ũ���ᷴӦ��������ͭ�����������ˮ����˶Ա�;��I����;����û�ж����������������Ⱦ��
a��;����IJ��������;����࣬����������Ⱦ��;����������Ⱦ�������������a����
b��;����2Cu+O2=2CuO��CuO+H2SO4=CuSO4+H2O��;������Cu+2H2SO4��Ũ��$\frac{\underline{\;\;��\;\;}}{\;}$ CuSO4+SO2��+2H2O��;�������;�����ʡԭ�ϣ��Ҳ�������Ⱦ����b��ȷ��
c��ͭԪ���غ��������ͬ�����ĵ���A��ȫ��Ӧ��������ͭ������ͬ����;���أ���c��ȷ��
d��2Cu+O2=2CuO��ÿ����1molBΪ����ͭ����ͭ��������Ӧ��������ͭ������0.5mol��������ת��2mol���ӣ���d����
�ʴ�Ϊ��bc��
��4��25g�������ʵ���=$\frac{25g}{250g/mol}$=0.1mol��������ȴ��������������������7.2g���ʵ���=$\frac{7.2g}{18g/mol}$=0.4mol�����CuSO4•5H2O��ѧʽ��֪��1molCuSO4•5H2Oʧȥ�Ľᾧˮ4mol���õ�����Ļ�ѧʽΪCuSO4•H2O��
�ʴ�Ϊ��CuSO4•H2O��
���� ���⿼���������Ʊ��ķ��������̷����жϣ���Ҫ���Ʊ����ʵIJ��衢������ƺ��������������ջ����ǽ���ؼ�����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ģ��Ϊ ��ij�л����� ��ij�л����� | B�� | ij����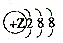 | ||
| C�� | ${\;}_{11}^{23}$M+ | D�� | 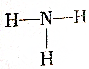 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Cl2��I2��S | B�� | Cl2��S��I2 | C�� | I2��Cl2��S | D�� | S��I2��Cl2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ������F-���ӣ�1mo1B�����ܴ��������û���3g��������ʱBת��Ϊ��Neԭ�Ӿ�����ͬ���Ӳ�ṹ�����ӣ���BԪ����Al��B�����������Ķ�Ӧˮ����Ļ�ѧʽΪAl��OH��3��CԪ����3�����Ӳ㣬��������Ӳ��L���Ӳ���2�����ӣ���CԪ����SC��Na��Ӧ��������ĵ���ʽΪ
������F-���ӣ�1mo1B�����ܴ��������û���3g��������ʱBת��Ϊ��Neԭ�Ӿ�����ͬ���Ӳ�ṹ�����ӣ���BԪ����Al��B�����������Ķ�Ӧˮ����Ļ�ѧʽΪAl��OH��3��CԪ����3�����Ӳ㣬��������Ӳ��L���Ӳ���2�����ӣ���CԪ����SC��Na��Ӧ��������ĵ���ʽΪ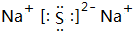 ���������еĻ�ѧ���������Ӽ���
���������еĻ�ѧ���������Ӽ����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٣��ڣ��� | B�� | �ڣ��٣��� | C�� | �ۣ��٣��� | D�� | �ڣ��ۣ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �٢ݢ� | C�� | �٢ۢ� | D�� | �ۢݢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com