
| A、①②④ | B、③④⑥ |
| C、②⑤⑥ | D、②④⑥ |
| ||


 津桥教育暑假拔高衔接广东人民出版社系列答案
津桥教育暑假拔高衔接广东人民出版社系列答案 波波熊暑假作业江西人民出版社系列答案
波波熊暑假作业江西人民出版社系列答案 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案科目:高中化学 来源: 题型:
| A、+1 | B、+2 | C、+3 | D、+4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由水电离的c(H+)=10-4mol/L的溶液中:Fe2+、SO42-、K+、NO3- | ||
| B、由水电离的c(H+)=10-14mol/L的溶液中:Ca2+、Na+、HCO3-、NO3- | ||
C、
| ||
| D、c(Fe3+)=0.1mol/L的溶液中:Na+、K+、NO3-、SO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、游离余氯指的是Cl- |
| B、Cl-有害人体健康,含Cl-的饮料不能饮用 |
| C、游离余氯既不是电解质也不是非电解质 |
| D、游离余氯与水反应的生成物,对水的电离无影响 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、
| ||
B、
| ||
C、
| ||
D、
|
查看答案和解析>>
科目:高中化学 来源: 题型:
| 编号 | 实验操作 | 实验现象 | 解释与结论 |
| A | 将无水乙醇和浓硫酸按照体积比1:3加入烧瓶中迅速加热到170℃,将生成的气体通入酸性高锰酸钾溶液 | 烧瓶中溶液由无色变成棕色,最后变为褐色;产生的气体使KMnO4溶液退色 | 乙醇发生消去反应,气体中含有乙烯 |
| B | 淀粉溶液和稀H2SO4混合加热一会,冷却后滴加NaOH至碱性,再加新制的Cu(OH)2悬浊液混合后加热至沸腾 | 有红色沉淀产生 | 淀粉完全水解了,且水解产物有还原性 |
| C | 分别将甲苯和己烷加入盛有少量酸性高锰酸钾溶液中,充分振荡 | 加甲苯的试管溶液颜色退去;加入己烷的试管溶液颜色没有退色 | 甲苯中的甲基可以被酸性高锰酸钾氧化,烷烃中的不能;有机物分子中原子(团)间的相互影响会导致物质化学性质的不同 |
| D | 将某卤代烃滴加到少量的NaOH溶液中充分振荡,然后再滴加几滴硝酸银溶液 | 有白色沉淀生成 | 该卤代烃属于氯代烃 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、用块状固体反应物代替粉末状反应物 |
| B、提高设备抗压强度以便加压 |
| C、采用高温高压的反应条件 |
| D、选择合适的催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
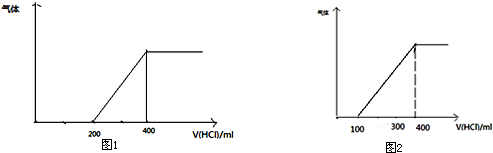
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com