
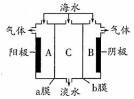
 海水中含有大量Na+、C1-及少量Ca2+、Mg2+、SO42-,用电渗析法对该海水样品进行淡化处理,如图所示.下列说法正确的是( )
海水中含有大量Na+、C1-及少量Ca2+、Mg2+、SO42-,用电渗析法对该海水样品进行淡化处理,如图所示.下列说法正确的是( )| A. | b膜是阳离子交换膜 | |
| B. | A极室产生气泡并伴有少量沉淀生成 | |
| C. | 淡化工作完成后A、B、C三室中pH大小为pHA<pHB<pHC | |
| D. | B极室产生的气体可使湿润的KI淀粉试纸变蓝 |
分析 A.电解时,阴离子向阳极移动,阳离子向阴极移动;
B.A极为阳极,发生氧化反应生成氯气;
C.B极生成氢气和氢氧根离子,pH最大;
D.B极为阴极,生成氢气.
解答 解:A.电解时,阴离子向阳极移动,阳离子向阴极移动,B为阴极,则b为阳离子交换膜,故A正确;
B.A极为阳极,发生氧化反应生成氯气,但没有沉淀生成,故B错误;
C.B极生成氢气和氢氧根离子,pH最大,应为pHA<pHC<pHB,故C错误;
D.B极为阴极,生成氢气,不能使湿润的KI淀粉试纸变蓝,故D错误.
故选A.
点评 本题综合考查水的净化、电解原理,为高频考点,侧重考查学生的分析能力,明确电解原理、物质的性质及发生的化学反应、化学用语的应用即可解答,题目难度不大.


科目:高中化学 来源: 题型:解答题

 ,
,查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在50g质量分数为46%的乙醇水溶液中,含有氢原子数为3NA | |
| B. | 80℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.2NA | |
| C. | lmol有机物CH3-CH=CH-CH2-CH3中最多有9NA个原子在同一平面上 | |
| D. | l04g苯乙烯(C6H5-CH=CH2)中含有8NA的碳氢键和4NA的碳碳双键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
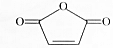
| A. | 分子式为C4H2O3 | B. | 能发生水解反应 | ||
| C. | 一氯代物有2种 | D. | 能使酸性KMnO4溶液褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
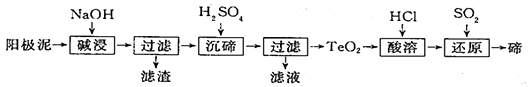
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | v(正)减小,v(逆)增大 | B. | v(正)增大,v(逆)减小 | C. | v(正)、v(逆)都减小 | D. | v(正)、v(逆)都增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH4(g)+2NO2(g)?N2(g)+CO2(g)+2H2O(l)△H<-867.0 KJ•mol-1 | |
| B. | 若增加甲烷的用量,平衡后体系中CO2的百分含量不一定升高 | |
| C. | 使用催化剂,可以降低反应的活化能,减少反应所放出的热量 | |
| D. | 标准状况下4.48 L CH4参加反应,转移电子数为1.6 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 候氏制碱、制取肥皂的工艺过程中均应用了物质溶解度的差异 | |
| B. | “青蒿一握,以水二升渍,绞取汁”,屠呦呦提取青蒿素的过程中发生了化学变化 | |
| C. | “外观如雪,强烧之,紫青烟起”,南北朝陶弘景对硝酸钾的鉴定过程中利用了焰色反应 | |
| D. | 使用可再生资源、用超临界二氧化碳替代有机溶剂、注重原子的经济性、采用低能耗生产工艺等都是绿色化学的内容 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
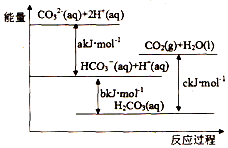
| A. | H2CO3(aq)=CO2(g)+H2O(l)为放热反应 | |
| B. | CO32-(aq)+H+(aq)=HCO3-(aq)△H=akJ/mol | |
| C. | HCO3-(aq)+H+(aq)=CO2(g)+H2O(l)△H=(c-b)kJ/mol | |
| D. | CO32-(aq)+2H+(aq)=CO2(g)+H2O(l)△H=(a+b-c)kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com