
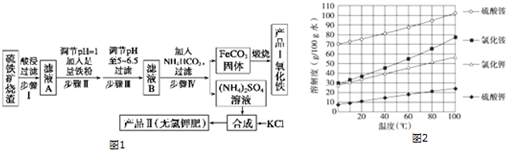
分析 Fe2O3、Fe3O4、FeO与还原剂反应生成铁,铁和稀硫酸反应生成硫酸亚铁和氢气,过滤时用到的仪器有铁架台、漏斗、烧杯、玻璃棒等,所以滤液中的主要溶质是硫酸亚铁;硫酸亚铁与碳酸氢铵反应得到碳酸亚铁和硫酸铵,实验室进行煅烧操作所需仪器有酒精灯、泥三角、三脚架、玻璃棒、坩埚、坩埚钳;碳酸亚铁与氧气反应生成了氧化铁盒二氧化碳;硫酸铵与氯化钾反应生成硫酸钾和氯化铵,根据硫酸钾的溶解度随温度变化不大,可用蒸发结晶、趁热过滤、洗涤、干燥得到硫酸钾,检验产品II中是否含有氯化物杂质需先除去SO4,再检验Cl-,以此解答该题.
解答 解:(1)酸浸时Fe2O3、Fe3O4、FeO能与稀硫酸反应得到Fe2+、Fe3+,SiO2不能与稀硫酸反应,因此酸浸、过滤后滤液A中含有的金属阳离子是Fe2+、Fe3+,
故答案为:Fe2+、Fe3+;
(2)滤液B含有硫酸亚铁,加入NH4HCO3溶液生成碳酸亚铁沉淀,反应的离子方程式为Fe2++2HCO3-=FeCO3↓+CO2↑+H2O,
故答案为:Fe2++2HCO3-=FeCO3↓+CO2↑+H2O;
(3)由流程图可知,煅烧FeCO3生成产品Ⅰ氧化铁和二氧化碳,Fe元素化合价升高,反应物中应有氧气,化学方程式为4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2,
故答案为:4FeCO3+O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+4CO2;
(4)硫酸铵与氯化钾反应生成硫酸钾和氯化铵;因硫酸钾的溶解度随温度变化不大,可用蒸发结晶、趁热过滤、洗涤、干燥得到硫酸钾,
故答案为:K2SO4;蒸发结晶;
(5)因检验产品II中是否含有氯化物杂质需先除去SO42-,再检验Cl-,所以滴加过量Ba(NO3)2溶液,过滤后向滤液滴加AgNO3溶液,
故答案为:滴加过量Ba(NO3)2溶液、AgNO3溶液;
(6)步骤Ⅲ中可选用氨水试剂调节溶液的pH.稀硝酸、双氧水、高锰酸钾溶液具有强氧化性,氧化亚铁离子,选择氨水调节除去杂质得到亚铁盐溶液,
故答案为:C.
点评 本题考查物质的制备和分离操作,侧重于学生分析能力、实验能力和综合运用化学知识能力的考查,为高考常见题型,题目难度中等,注意根据实验流程以及相关物质的性质解答该题.


科目:高中化学 来源: 题型:多选题
| A. | 用带橡皮塞的棕色试剂瓶存放浓硝酸 | |
| B. | 容量瓶、分液漏斗使用前均需检查是否漏水 | |
| C. | 分液漏斗分液时,必须先将下层液体从下口放出,再将上层液体从上口倒出 | |
| D. | 蒸馏时,需将温度计的水银球没入液面以下且不接触烧瓶壁 | |
| E. | 氨气喷泉实验时,收集气体的烧瓶必须干燥 | |
| F. | 用玻璃棒蘸取待测液,点在润湿的pH试纸上测定其pH |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 (1)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图.该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为NO2+NO3--e-═N2O5.若生成1molY,则需要消耗标准状况下氧气的体积为5.6L.
(1)NO2、O2和熔融NaNO3可制作燃料电池,其原理如图.该电池在使用过程中石墨I电极上生成氧化物Y,其电极反应式为NO2+NO3--e-═N2O5.若生成1molY,则需要消耗标准状况下氧气的体积为5.6L.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
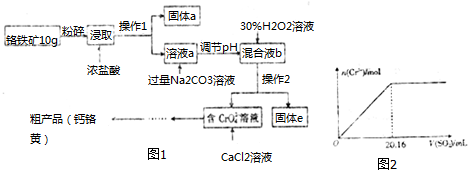
| 氢氧化物 | Ksp | 开始沉淀时的pH | 沉淀完全的pH |
| Fe(OH)3 | 2.5×10-38 | 2.3 | 3.5 |
| Fe(OH)2 | 1.0×10-15 | 7.5 | 9.5 |
| Al(OH)3 | 2.0×10-32 | 4.0 | 5.4 |
| Cr(OH)3 | 5.4×10-31 | 4.6 | 5.9 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④⑦ | B. | .①②③④⑤ | C. | .①②③⑥⑧ | D. | .③④⑦⑧⑨ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA | |
| B. | 标准状况下,22.4L盐酸含有NA个HC1分子 | |
| C. | 1Lmol•L-1的NaC1O溶液中含有C1O-的数目为NA | |
| D. | 1molNa被完成氧化生成Na2O2,失去个2NA电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaHSO4 | B. | Al2(SO4)3 | C. | NaOH | D. | HCl |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com