
| A. | 油脂 | B. | 合成橡胶 | C. | 聚乙烯 | D. | 蛋白质 |
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源: 题型:选择题
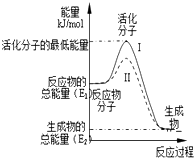
| A. | 每当生成2molNH3(g)要吸收92kJ的能量 | |
| B. | 每当生成2mol NH3(g)要释放92kJ的能量 | |
| C. | 每当生成2mol NH3(g)要吸收561kJ的能量 | |
| D. | 每当生成2mol NH3(g)要释放561kJ的能量 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③④ | B. | ①③⑤ | C. | ②④⑥ | D. | ①②③⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 一定温度下,1L0.5mol•L-1NH4Cl溶液与1L0.25mol•L-1NH4Cl溶液中NH4+物质的量之比为2:1 | |
| B. | 100g硫酸溶液的物质的量浓度为18.4mol/L,用水稀释到物质的量浓度为9.8mol/L,需要水100g. | |
| C. | 标准状况下,22.4LCH3Cl和CHCl3的混合物中所含有的碳原子个数一定为NA | |
| D. | 在2Na2O2+2CO2=2Na2CO3+O2反应中,每生成16g氧气,则转移NA个电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
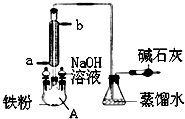
| A. | 仪器A左上侧的分液漏斗中加入的是苯和溴水 | |
| B. | 仪器A的名称叫蒸馏烧瓶 | |
| C. | NaOH溶液的主要作用是除去反应后溶解在溴苯中的溴 | |
| D. | 碱石灰作用是防止空气中水蒸气进入反应体系 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ②③④⑤ | B. | ①③④⑤ | C. | ①②③④ | D. | ①②④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 .
.
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 (1)已知:
(1)已知:查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com