
һ������CO2��������̼������ɱ�ĺ�ѹ�ܱ������з�Ӧ��C��s��+CO2��g�� 2CO��g����ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��
2CO��g����ƽ��ʱ����ϵ����������������¶ȵĹ�ϵ����ͼ��ʾ��

��֪�������ѹ��P�֣�=������ѹ��P�ܣ����������������˵����ȷ����
A��550��ʱ��������������壬v����v�����С��ƽ�ⲻ�ƶ�
B��T��ʱ��������������CO2��CO��ƽ�����淴Ӧ�����ƶ�
C��650��ʱ����Ӧ��ƽ���CO2��ת����Ϊ25��0%
D��925��ʱ����ƽ���ѹ����ƽ��Ũ�ȱ�ʾ�Ļ�ѧƽ�ⳣ��KP=24��0P��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������������ѧ�߶��ϵ�һ���¿���ѧ�Ծ��������棩 ���ͣ������
��֪�����Ȼ�ѧ����ʽ��
��H2O��l����H2��g����1/2O2��g�� ��H1����285��8kJ/mol
��H2��g����1/2O2��g����H2O��g�� ��H2����241��8kJ/mol
��C��s����1/2O2��g����CO��g�� ��H3����110��5kJ/mol
��C��s����O2��g����CO2��g�� ��H4����393��5kJ/mol
�ش��������⣺
��1��C��ȼ����Ϊ
��2��ȼ��10gH2����Һ̬ˮ���ų�������Ϊ
��3��д��COȼ�յ��Ȼ�ѧ����ʽ
��4��д����ˮú�����Ȼ�ѧ����ʽ ��4�֣�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���������һ�и߶������в����Ŀƻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
�����Լ��У��ܰ�ϡ���ᡢˮ�Ͱ�ˮ������ɫҺ�����ֿ�����
��A��pH��ֽ ��B����̪��Һ ��C��ϡ���� ��D���Ȼ�����Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ��У��������ѧ��10�½β⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ��������ʵ�������ȷ����
A��Ư����Һ�ڿ�����ʧЧ��ClO- + CO2 + H2O ==== HClO + HCO3-
B����Ũ������MnO2��Ӧ��ȡ����������
MnO2+2H++2Cl-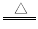 Mn2++Cl2��+2H2O
Mn2++Cl2��+2H2O
C����Na��Al��OH��4����Һ��ͨ�����CO2��Al��OH��3��
��Al��OH��4��- + CO2 ==== Al��OH��3�� + HCO3-
D����ǿ����Һ�д���������Fe��OH��3��Ӧ����Na2FeO4��
3ClO-+2Fe��OH��3====2FeO42-+3Cl-+H2O+4H+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ɽ��ʡ������10�½��ʼ컯ѧ�Ծ��������棩 ���ͣ�ѡ����
�ö��Ե缫���ú��Һ�ķ�����H2�ķ�ӦΪC��s��+2H2O��l��=CO2��g��+2H2��g�����ֽ�һ������1mol/LH2SO4��Һ������ú�۳�ֻ�ϣ��Ƴɺ�̼��Ϊ0��02g/mL~0��12g/mL��ú��Һ��������ͼ��ʾװ���н��е�⣨���缫��Ϊ���Ե缫��������˵���������

A��A����������B������
B��A���ĵ缫��ӦʽΪC+2H2O-4e-=CO2��+4H+
C��B���ĵ缫��ӦʽΪ2H++2e-=H2��
D�����һ��ʱ���ú��Һ��pH����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�������������ѧ�߶���9���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
21�����������ɡ���ʯ��Դʱ����������Դʱ�������ɣ����в���������Դ����
A��̫���� B������ C������ D������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�����ѧ�ڵ������¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��һ������������ȫ�ܽ���ijŨ�ȵ������У���Ӧ���ռ���NO2��NO�Ļ�����壬����˵����ȷ����
A����Ӧ�����ɵ���ֻ��Fe��NO3��2
B����Ӧ�����ɵ���ֻ��Fe��NO3��3
C����Ӧ�����ɵ���ΪFe��NO3��2��Fe��NO3��3
D������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�����ɹŰ������߶���10���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪���������Ȼ�ѧ����ʽ
2H2��g��+ O2��g��===2H2O��l����H = -571��6kJ��mol-1
C3H8��g��+5O2��g��=== 3CO2��g��+ 4H2O��l����H = -2 220��0kJ��mol-1
ʵ���������ͱ���Ļ�����干5 mol��ȫȼ��ʱ����3847kJ�����������������������������
A��1:3 B��3:1 C��1:4 D��1:1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�콭��ʡ������ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��ʾ��װ�÷ֱ��������ʵ�飬�������ʷ�Ӧ����Һ�ĵ����Աȷ�Ӧǰ������ǿ����
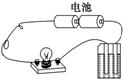
A��������������Һ��ͨ��������Na2SO3��Cl2��H2O===Na2SO4��2HCl
B������������Һ��ͨ�������Ȼ��⣺AgNO3��HCl===AgCl����HNO3
C�������ⱥ����Һ��ͨ������������2H2S��O2===2H2O��2S��
D����NaOH��Һ��ͨ������������2NaOH��Cl2===NaCl��NaClO��H2O
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com