

 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
组别 | 通入气体 | 控制温度 |
A | CO2 | 30—40 ℃ |
B | CO2 | 0—10 ℃ |
C | NH3 | 30—40 ℃ |
D | NH3 | 0—10 ℃ |
查看答案和解析>>
科目:高中化学 来源: 题型:
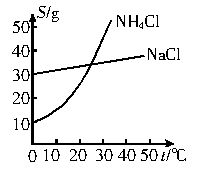
联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl。NaCl和NH4Cl共同存在时的溶解度曲线如下图所示,则正确的操作是
查看答案和解析>>
科目:高中化学 来源: 题型:
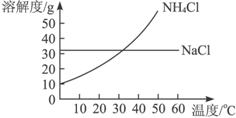
联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl。NaCl和NH4Cl共同存在时的溶解度曲线如下图所示,则正确的操作是
查看答案和解析>>
科目:高中化学 来源:2013届浙江省高二上学期第一次月考化学试试卷二(解析版) 题型:选择题
联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl。NaCl和NH4Cl共同存在时的溶解度曲线如下图所示,则正确的操作是

查看答案和解析>>
科目:高中化学 来源:2010年辽宁省本溪县高一上学期10月月考化学试题 题型:选择题
联合制碱法中关键的一步是把NH4Cl从几乎饱和的NaHCO3溶液中分离出来,为此根据NaCl和NH4Cl溶解度的差异,向混合溶液中通入某种气体,同时加入磨细的食盐,可析出不夹带NaHCO3的NH4Cl。NaCl和NH4Cl共同存在时的溶解度曲线如下图所示,则正确的操作是

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com