
| A. | 氢 | B. | 钠 | C. | 铁 | D. | 氯 |
科目:高中化学 来源: 题型:推断题
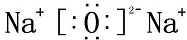 ;水溶液PH=8,则C(HY-)+2C(H2Y)=10-6-10-8mol/L(填精确值).
;水溶液PH=8,则C(HY-)+2C(H2Y)=10-6-10-8mol/L(填精确值).查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用10 mL量筒量取5.80 mL 乙醇溶液 | |
| B. | 乙酸的酯化反应实验中用NaOH溶液除去生成物中的乙酸 | |
| C. | 用溴水可以除去乙烷中的乙烯 | |
| D. | 食盐可以鉴别白酒和食醋 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 根据置换反应Na+KCl$\frac{\underline{\;高温\;}}{\;}$NaCl+K↑,推出金属Na的活泼性强于金属K的活泼性 | |
| B. | 根据主族元素最高正化合价与族序数的关系,推出卤族元素最高正价都是+7 | |
| C. | 根据金属活动顺序表推知Sn活泼性强于Pb,推出碱性Sn(OH)4>Pb(OH)4 | |
| D. | 根据较强酸可以制取较弱酸的规律,推出CO2通入NaClO溶液中能生成HClO |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H5OH在电池的负极上参加反应 | |
| B. | 1 mol乙醇被氧化转移6 mol电子 | |
| C. | 在外电路中电子由负极沿导线流向正极 | |
| D. | 电池正极得电子的物质是O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 实验 | 现象 |
| A | 加热放在坩埚中的小块钠 | 钠先熔化成光亮的小球,燃烧时火焰为黄色,燃烧后生成淡黄色固体 |
| B | 在酒精灯上加热铝箔 | 铝箔熔化,失去光泽,熔化的铝滴落下来 |
| C | 向久置于空气中的FeSO4溶液中滴加NaOH溶液 | 立刻产生大量白色沉淀 |
| D | 向饱和Na2CO3溶液中通入足量的CO2气体 | 无明显现象 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com