

���� ��1�����ʳ��ˮ����NaOH��H2��Cl2���Դ���д���ӷ���ʽ��
A�������ӽ���Ĥֻ������������ͨ����
B������ͼ֪����߰��������ӷŵ������������ұ߰��������ӷŵ�������������X��������Y��������
C�����������������ӷŵ磻
D����������Ϊ�����ң�
��2���������Ȼ��õ����Ȼ��ѡ��Ȼ�����һ����̼������ԭ���غ���ƽд�������ݵ�ʧ���Ӽ�������2 mol���Ȼ���ʱת�Ƶĵ��ӵ����ʵ�����
��3��ԭ����и�����ȼ��ʧ���ӣ����������£�CH3OH��Ӧ����̼������ӣ�
��4����Ar���н��з�ֹ�ѡ�þ�������������¶�ʹTiCl4��Mg��MgCl2ת��Ϊ������Ti���ڻ���
��5�����ȸ���ȼ���ȷֱ�д��CO��H2��CH3OH�Ȼ�ѧ����ʽ���ݸ�˹���ɾͿɵó�CO��H2�ϳɼ״����Ȼ�ѧ����ʽ��
�ڸ��ݼ״������ʵ���������ҪCO��H2�����ʵ���������n��CO�������������ɵ�n��Cl2������������������n��H2�����ݴ˼�����
��� �⣺��1�����ʳ��ˮ����NaOH��H2��Cl2����Ӧ�����ӷ���ʽΪ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����
A�������ӽ���Ĥֻ������������ͨ���������Ӻͷ��Ӳ���ͨ������A����
B������ͼ֪����߰��������ӷŵ������������ұ߰��������ӷŵ�������������X��������Y����������B����
C�����������������ӷŵ磬�缫��ӦʽΪ2H++2e-�TH2������C��ȷ��
D�����������е缫Ϊ����������Ϊ�����ң�����Ϊ�����ң���D����
�ʴ�Ϊ��2Cl-+2H2O$\frac{\underline{\;���\;}}{\;}$2OH-+H2��+Cl2����C��
��2����ͼʾ��֪�Ȼ�ʱ�ķ�Ӧ��ΪFeTiO3��C��Cl2��������ΪFeCl3��TiCl4��CO���ٸ��ݵ�ʧ���Ӻ�ԭ���غ㼴�ɵó��÷�Ӧ�ķ���ʽΪ2FeTiO3+6C+7Cl2$\frac{\underline{\;����\;}}{\;}$2FeCl3+2TiCl4+6CO���ɷ���ʽ�ó�����2molTiCl4ת��14mol���ӣ���������2mol���Ȼ���ʱת�Ƶ��ӵ����ʵ���Ϊ14mol��
�ʴ�Ϊ��2FeTiO3+6C+7Cl2$\frac{\underline{\;����\;}}{\;}$2FeCl3+2TiCl4+6CO��14��
��3��ԭ��طŵ�ʱ���״�ʧ���ӱ�������ӦΪ��ظ�����Ӧ����缫��ӦʽΪ��2CH3OH+3O2+4OH-=2CO32-+6H2O��
�ʴ�Ϊ��CH3OH+8OH--6e-=CO32-+6H2O��
��4����Ar���н��з�ֹ�ѡ�þ�����������������ã�
�ʴ�Ϊ�����������ã�
��5����COȼ�յ��Ȼ�ѧ����ʽ��H2ȼ�յ��Ȼ�ѧ����ʽ��2H2��g��+O2��g���T2H2O��l����H=-285.8��2 kJ•mol-1 ��
CO��g��+$\frac{1}{2}$O2��g���TCO2��g����H=-283kJ•mol-1��
CH3OHȼ�յ��Ȼ�ѧ����ʽ��CH3OH��l��+$\frac{3}{2}$O2��g���TCO2��g��+2H2O��l����H=-726.5kJ•mol-1 ��
���ݸ�˹���ɽ���+��+��-�ۣ��ɵã�CO��g��+2H2��g���TCH3OH��l����H=-128.1KJ•mol-1��
�ʴ�Ϊ��CO��g��+2H2��g���TCH3OH��l����H=-128.1KJ•mol-1��
����CO��g��+2H2��g��?CH3OH��g����֪���ϳ�6mol�״���Ҫn��CO��=6mol��n��H2��=12mol������2FeTiO3+6C+7Cl2$\frac{\underline{\;����\;}}{\;}$2FeCl3+2TiCl4+6CO��֪����������ɵ�n��Cl2��=$\frac{7}{6}$n��CO��=7mol������2NaCl+2H2O$\frac{\underline{\;���\;}}{\;}$2NaOH+H2��+Cl2����֪���������n��H2��=n��Cl2��=7mol��������ⲹ��H2 Ϊ12mol-7mol=5mol��V=5��22.4=112L��
�ʴ�Ϊ��112��
���� �������ȼҵΪ���忼���˵���ԭ���������˻�ѧ����ʽ����д�����㡢��˹���ɵȣ�ע�⣨1�������ͼ������Ũ�ȱ仯ȷ���缫�����ķ�ӦΪ�Ȿ��ؼ���֪�����ӽ���Ĥ�����á������缫�Ϸ����ķ�Ӧ����Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH2=CH-CH=CH2 | B�� | CH2=CH-C��CH | C�� | 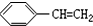 | D�� | 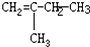 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
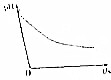 ij���ӷ�Ӧ�漰H2O��CLO-��NH4+��H+��N2��CL-�����������������·�Ӧʱ����ҺpH��ʱ��仯��������ͼ��ʾ�������жϴ�����ǣ�������
ij���ӷ�Ӧ�漰H2O��CLO-��NH4+��H+��N2��CL-�����������������·�Ӧʱ����ҺpH��ʱ��仯��������ͼ��ʾ�������жϴ�����ǣ�������| A�� | �÷�Ӧ����������CLO- | |
| B�� | �÷�Ӧ���������������� | |
| C�� | �÷�Ӧ����1mol��������ʱ��ת�Ƶĵ���Ϊ6mol | |
| D�� | �μӷ�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ2��3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Ԫ��W�����γ�ԭ�ӱ�Ϊ1��1�Ļ������ж��� | |
| B�� | Ԫ��X�ĵ�������ˮ����ˮ�Ҵ���Ӧ | |
| C�� | ����Y3+��Z-�������������͵��Ӳ���������ͬ | |
| D�� | Ԫ��W��Ԫ��Z���γɺ��м��Թ��ۼ��Ļ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
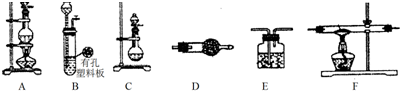
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 56g Fe��ϡHNO3��ȫ��Ӧʱһ��ת��3NA������ | |
| B�� | ��״����11.2 L NH3����1 Lˮ�У���Һ�к�Nԭ�ӵ�������Ϊ0.5NA | |
| C�� | ���³�ѹ�£�0.1NA��Al����������������Һ��Ӧ����3.36 LH2 | |
| D�� | ͬ��ͬѹ�£�H2��g��+Cl2��g��=2HCl��g���ڹ��պ͵�ȼ�����µġ�H��ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | Na+��Cl-��HCO3-��Ca2+ | B�� | OH-��Na+��Mg2+��HCO3- | ||
| C�� | Na+��Cl-��H+��Ag+ | D�� | Na+��SiO32-��H+��Cl- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢� | B�� | �ڢ� | C�� | �ڢۢݢ� | D�� | �٢ڢۢܢݢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com