
下列叙述正确的是( )
A.SO2使溴水褪色与乙烯使KMnO4溶液褪色的原理不同
B.向FeCl2溶液中滴加氯水,溶液颜色变成棕黄色,说明氯水中含有HClO
C.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能增大生成H2的速率
D.用AgNO3溶液可以鉴别KCl和KI
科目:高中化学 来源: 题型:
G是黄酮类药物的主要合成中间体,
可由A( ﹣CH=CH2)和D(HO﹣
﹣CH=CH2)和D(HO﹣ ﹣CHO)按如下方法合成:
﹣CHO)按如下方法合成:
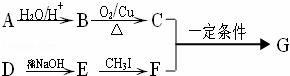
已知以下信息:
①C不能发生银镜反应.
② ﹣ONa+RCH2I→
﹣ONa+RCH2I→ ﹣OCH2R+NaI
﹣OCH2R+NaI
③RCOCH3+R′CHO RCOCH=CHR'
RCOCH=CHR'
回答下列问题:
(1)A的化学名称为 ,1mol A最多可跟 mol H2发生反应.
(2)D的含氧官能团的名称是 ,由E生成F的反应类型为 .
(3)由B生成C的化学方程式为 .
(4)G的结构简式为 .
(5)H是F的同分异构体,符合下列条件,写出H的结构简式 .
①能发生银镜反应.
②能与FeCl3溶液发生显色反应.
③苯环上有2个取代基,核磁共振氢谱有5个峰,强度比为1:1:2:2:2.
查看答案和解析>>
科目:高中化学 来源: 题型:
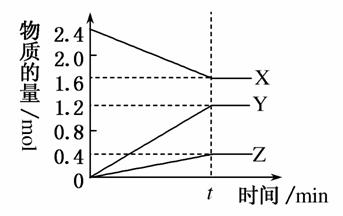
在2 L容器中3种物质间进行反应,X、Y、Z的物质的量随时间变化曲线如图。反应在t时刻达到平衡,依图所示:
(1)该反应的化学方程式是_____________________________。
(2)反应起始至t,Y的平均反应速率是_____________________ _________________________________________________。
(3)X的转化率是_____________________________________。
(4)关于该反应的说法正确的是________。
A.到达t时刻反应已停止
B.在t时刻之前X的消耗速率大于它的生成速率
C.在t时刻正反应速率等于逆反应速率
D.在t时刻达到平衡是因为此时反应物总物质的量与生成物总物质的量相等
查看答案和解析>>
科目:高中化学 来源: 题型:
已知氯气的漂白作用实际上是氯气与水反应生成的次氯酸的漂白作用。为了探究SO2的漂白作用到底是SO2本身还是SO2与水作用的产物,某学习小组设计了如图装置来进行实验。请回答相关问题。
(1)制备SO2气体的反应方程式为: ;
发生装置的玻璃仪器名为 、 ;
(2)为了探究干燥的SO2能不能使品红褪色,某同学设计了如图所示实验装置,请指出实验装置图设计中的不合理之处。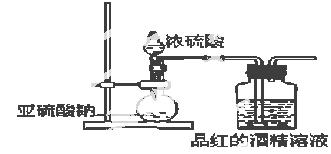
① ;② ;
(3)按照修改后的装置,实验中控制SO2以大约每秒3个气泡的速度通过品红的酒精溶液时,经过一小时后,品红仍不褪色.这说明品红褪色的原因不是SO2直接导致。为此,SO2能使品红的水溶液褪色的可能微粒有(不考虑水及水电离出来的粒子) 。
(4)甲同学实验如下:取等量、相同浓度的品红水溶液于两支试管中,再分别加入少量Na2SO3固体和NaHSO3固体,两支试管中的品红都褪色,对此他得出结论:使品红褪色的微粒是HSO3-和SO32-,不是H2SO3。你认为他的结论是否正确 ,其理由是 。
(5)为了进一步探究,乙组同学做了如下实验:分别取相同浓度的品红水溶液各20ml于两只小烧杯中,再分别一次性加入20ml 0.1mol/L的Na2SO3溶液、20ml 0.1mol/L的NaHSO3溶液,发现加入Na2SO3溶液的品红褪色较快。
①微粒浓度与褪色快慢关系,请用“多”或“少”填写“ ”内容:
| 同浓度溶液 | SO32- | HSO3- | H2SO3 | 褪色速度 |
| Na2SO3溶液 | 多 | 少 | 少 | 快 |
| NaHSO3溶液 | 较上面_________ | 较上面_______ | 较上面_______ | 慢 |
②根据实验和分析,得出的结论是
查看答案和解析>>
科目:高中化学 来源: 题型:
适用相关化学知识进行判断,下列结论正确的是
A.某吸热反应能自发进行,则该反应的△S>0
B.SO2使酸性KMnO4溶液褪色,因此SO2具有漂白性
C.在物质分离的方法中,蒸馏、萃取、重结晶都与物质的溶解度有关
D.增大反应物浓度可加快反应速率,因此用浓硫酸与铁反应能加快生成H2的速率
查看答案和解析>>
科目:高中化学 来源: 题型:
SiO2、SO2和CO2都是酸性氧化物,它们的化学性质有一定的相似性;Mg和Na的化学性质也有一定相似性。某兴趣小组用如图所示装置进行Mg与SO2反应的实验。
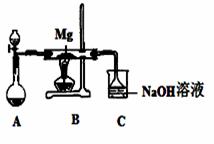
(1)选择制取SO2的合适试剂 (填编号)。
①浓HCl ②浓H2SO4
③Na2SO3固体 ④CaSO3固体
(2)上述装置还可改进,改进的方法是
,
若C中NaOH为0.2mol/L、200ml,通入的SO2为1.12L(标准状况),则该反应的离子方程式为
(3)甲同学推测Mg与SO2的反应与CO2相似,则该反应方程式为
乙同学的推测是:2Mg+3SO2 2MgSO3+S;
2MgSO3+S;
丙同学的推测是:3Mg+SO2 2MgO+MgS,
2MgO+MgS,
要验证甲、乙、丙三位同学的推测是否正确,丁同学作如下实验探究:
已知:MgSO3和MgS都是微溶于水,能与盐酸发生复分解反应放出气体;
限选试剂:2mol/L HCl、2mol/L HNO3、蒸馏水、2mol/L NaOH、品红溶液、澄清石灰水、2mol/L CuSO4;仪器和用品自选。请填写下表中的空格:
根据上述实验探究:
| 序号 | 实验步骤 | 预期现象和结论 |
| ① | 取少量反应后的固体于试管I中 |
|
| ② | 向试管I中的固体慢慢滴加 试管I口塞上带导管的单孔塞,并将导管通入盛有 的试管II中。 | 若试管I中的 , 则丙同学推测正确。若试管I中的固体未完全溶解,且 ,则乙同学的推测正确。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质中,不满足组内任意两种物质在一定条件下均能发生反应的是( )
| 组别 | 甲 | 乙 | 丙 |
| A | Al(OH)3 | HCl | NaOH |
| B | NH3 | O2 | HNO3 |
| C | SO2 | Ca(OH)2 | NaHCO3 |
| D | O2 | N2 | H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com