
【题目】请参考题中图表,已知E1=134kJ/mol、E2=368kJ/mol,根据要求回答问题:
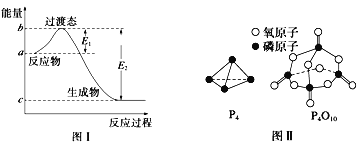
(1)图I是1molNO2(g)和1molCO(g)反应生成CO2和NO过程中的能最变化示意图,若在反应体系中加入催化剂,反应速率增大,E1的变化是___(填“增大”、“减小”或“不变”下同),△H的变化是________。请写出NO2和CO反应的热化学方程式:__________。
(2)如表所示是部分化学键的键能参数:
化学键 | P-P | P-O | O=O | P=O |
键能/kJ/mol | a | b | c | x |
已知白磷的燃烧热为dkJ/mol,白磷及其完全燃烧的产物的结构如图II所示。1个P4O10分子中P-O的个数为_______,表中x=_____kJ/mol(用含a、b、c、d的代表数式表示)。
【答案】减小不变NO2(g)+CO(g)=CO2(g)+NO(g) ΔH=-234 kJ·mol-112 (d+6a+5c-12b)/4
【解析】
(1)加入催化剂能降低反应所需的活化能,但是不改变反应物的总能量和生成物的总能量,由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,根据热化学方程式书写原则进行书写;
(2)白磷燃烧的方程式为P4+5O2=P4O10,根据化学键的断裂和形成的数目进行计算。
(1)加入催化剂能降低反应所需的活化能,则E1和E2都减小,催化剂不能改变反应物的总能量和生成物的总能量之差,即反应热不改变,所以催化剂对反应热无影响,由图可知,1mol NO2和1mol CO反应生成CO2和NO放出热量368-134=234kJ,反应热化学方程式为NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJmol-1,故答案为:减小;不变;NO2(g)+CO(g)=NO(g)+CO2(g)△H=-234 kJmol-1;
(2)白磷燃烧的方程式为P4+5O2=P4O10,根据图示,1mol白磷完全燃烧需拆开6mol P-P、5mol O=O,形成12molP-O、4mol P=O,所以12mol×bkJ/mol+4mol×xkJ/mol-(6mol×a kJ/mol+5 mol×c kJ/mol)=dkJ/mol,x=![]() kJ/mol,故答案为:12;
kJ/mol,故答案为:12;![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】锂离子电池已经成为应用最广泛的可充电电池。某种锂离子电池的结构示意图如下图所示,其中两极区间的隔膜只允许Li+通过。电池放电时的总反应方程式为:
Li1-xCoO2+xLi==LiCoO2。关于该电池的推论错误的是

A. 放电时,Li+主要从负极区通过隔膜移向正板区
B. 放电时,负极反应为:xLi-xe-=xLi+
C. 电解貭溶液不能是水溶液
D. 充电时,负极(C)上锂元素被氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化铅(PbO)是黄色固体。实验室用草酸在浓硫酸作用下分解制备CO,其原理为:H2C2O4![]() CO↑+CO2↑+H2O。某课题组同学设计实验探究CO还原氧化铅并检验氧化产物(已知CO能使银氨溶液产生黑色沉锭)的装置如图所示。下列说法正确的是
CO↑+CO2↑+H2O。某课题组同学设计实验探究CO还原氧化铅并检验氧化产物(已知CO能使银氨溶液产生黑色沉锭)的装置如图所示。下列说法正确的是

A. 实验时,先点燃装置①处酒精灯,当装置⑤中产生连续气泡且有明显现象后再点燃装置③处酒精灯
B. 装置②④⑤中的试剂依次为碱石灰、银氨溶液、澄清石灰水
C. 实验完毕时,先熄灭装置①处酒精灯,再熄灭装置③处酒精灯
D. 尾气处理可选用点燃、气袋收集、NaOH溶液吸收等方法
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有四种原子:①![]() ②
②![]() ③
③![]() ④
④![]()
(1)其中能与②形成离子键的是___________(填序号)。
(2)①的核外电子数是____;①和②形成的化学键是_____(填“极性键”或“非极性键”)。
(3)②和③互为同位素的本质原因是___________。
(4)④的原子结构示图是______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为测定某氟化稀土样品中氟元素的质量分数,某化学兴趣小组进行如下了实验。
利用高氯酸(高沸点酸)将样品中的氟元素转化为氟化氢(低沸点酸)蒸出,再通过滴定测量。
实验装置如图所示。

(1)a的作用是____________,仪器d的名称是________________ 。
(2)检查装置气密性:____________(填操作),关闭k,微热c,导管e末端有气泡冒出;停止加热,导管e内有一段稳定的水柱,说明装置气密性良好。
(3)c中加入一定体积高氯酸和mg氟化稀土样品,Z中盛有滴加酚酞的NaOH溶液。加热b、c,使b中产生的水蒸气进入c。
①下列物质可代替高氯酸的是_________(填序号)。
A.硝酸 B.盐酸 C.硫酸 D.磷酸
②实验中除有HF气体外,可能还有少量SiF4(易水解)气体生成。若有SiF4生成,实验结果将__________(填“偏高”“ 偏低”或“不受影响”)。
③若观察到f中溶液红色褪去,需要向f中及时补加NaOH溶液,否则会使实验结果偏低,原因是______________。
(4)向馏出液中加入V1mL c1mol·L-1La(NO3)3溶液,得到LaF3沉淀,再用c2mol·L-1EDTA标准溶液滴定剩余La3+(La3+与EDTA按1:1络合),消耗EDTA标准溶液V2ml,则氟化稀土样品中氟的质量分数为______________。
(5)用样品进行实验前,需要用0.084g氟化钠代替样品进行实验,改变条件(高氯酸用量、反应温度、蒸馏时间),测量并计算出氟元素质量,重复多次。该操作的目的是___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一个化学电池的总反应方程式为:Zn+Cu2+═Zn2++Cu,该化学电池的组成可能为( )
A | B | C | D | |
正极 | Cu | Cu | Zn | Al |
负极 | Zn | Zn | Cu | Zn |
电解质溶液 | H2SO4 | CuSO4 | ZnCl2 | Cu Cl2 |
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关生活中常见有机物的说法不正确的是
A. 医用消毒酒精的体积分数为75%
B. 煤干馏的主要产品是煤油
C. 液化石油气和天然气的主要成分不同
D. 常用福尔马林溶液保存动物标本
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com