
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 第1周期 | ② | |||||||
| 第2周期 | ④ | ⑥ | ⑦ | |||||
| 第3周期 | ① | ③ | ⑤ | ⑧ | ⑨ | ⑩ |
 .
.分析 由元素在周期表中位置,可知①为Na、②为H、③为Mg、④为B、⑤为Al、⑥为C、⑦为N、⑧为S、⑨为Cl、⑩为Ar.
(1)稀有气体化学性质最不活泼;
(2)金属性越强,最高价氧化物对应水化物的碱性越强,氢氧化镁中含离子键和O-H共价键;
(3)②和⑦两元素形成四核化合物为氨气;
(4)同周期自左而右元素非金属性增强;根据单质与氢气反应难易、剧烈程度判断,根据氢化物稳定性、最高价含氧酸的酸性强弱、单质之间的相互置换反应、化合物中元素化合价等判断非金属性强弱;
(5)元素①的最高价氧化物的水化物为NaOH,⑤的最高价氧化物为Al2O3,二者反应生成偏铝酸钠和水;
(6)氯气与NaOH反应生成NaCl、NaClO和水.
解答 解:由元素在周期表中位置,可知①为Na、②为H、③为Mg、④为B、⑤为Al、⑥为C、⑦为N、⑧为S、⑨为Cl、⑩为Ar.
(1)稀有气体Ar的化学性质最不活泼,故答案为:Ar;
(2)③④⑤三种元素中Mg的金属性最强,故Mg(OH)2的碱性最强,含有离子键、共价键,
故答案为:Mg(OH)2;离子键、共价键;
(3)②和⑦两元素形成四核化合物为氨气,其电子式为 ,故答案为:
,故答案为: ;
;
(4)同周期自左而右元素非金属性增强,故非金属性Cl>S;
a.非金属性强弱与获得电子的难易程度有关,与获得电子数目多少无关,故a错误;
b.⑨的氢化物比⑧的氢化物稳定,说明⑨的非金属性更强,故b正确;
c.单质都能与氢氧化钠溶液反应不能比较元素非金属性强弱,若氧气不能与氢氧化钠溶液,而硫与氢氧化钠溶液反应,故c错误;
d.最高价氧化物对应水化物酸性⑨比⑧强,说明⑨的非金属性更强,故d正确,
故答案为:Cl;bd;
(5)元素①的最高价氧化物的水化物为NaOH,⑤的最高价氧化物为Al2O3,二者反应生成偏铝酸钠和水,离子反应为Al2O3+2OH-═2AlO2-+H2O,
故答案为:Al2O3+2OH-═2AlO2-+H2O;
(6)氯气与NaOH反应生成NaCl、NaClO和水,化学反应为Cl2+2NaOH=NaCl+NaClO+H2O,故答案为:Cl2+2NaOH=NaCl+NaClO+H2O.
点评 本题考查位置、结构与性质,为高频考点,把握元素的位置、性质、元素化合物知识为解答本题关键,侧重分析与应用能力的考查,注意化学用语、元素周期律及元素化合物的应用,综合性较强,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 用核磁共振氢谱不能鉴别1-丙醇和2-丙醇 | |
| B. | 实验证实 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 可使Br2的CCl4溶液褪色,说明该分子中存在独立的碳碳单键和碳碳双键 | |
| C. | 醋酸和硬脂酸互为同系物,C6H14和C9H20也一定互为同系物 | |
| D. | 淀粉水解实验:淀粉溶液中加入稀硫酸加热水解得水解液,再加入NaOH溶液得中和液,后加入新制Cu(OH)2悬浊液加热后有红色沉淀.结论:淀粉已水解 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Al3+的结构示意图: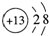 | |
| B. | 甲酸甲酯的结构简式:C2H4O2 | |
| C. | 醋酸的电离方程式:CH3COOH═CH3COO-+H+ | |
| D. | 中子数为145、质子数为94的钚(Pu)原子:${\;}_{94}^{145}$Pu |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
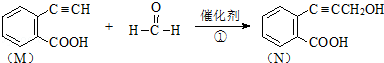
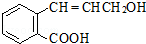 )发生缩聚反应产物的结构简式为
)发生缩聚反应产物的结构简式为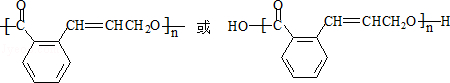 ;
; 有机物Ⅱ的结构简式为CH3C≡CCH=CHCH2CH3;A、B可以发生类似①的反应生成有机物Ⅰ,则该反应的化学方程式为CH3C≡CH+CH3CH2CHO$\stackrel{催化剂}{→}$CH3C≡CCH(OH)CH2CH2CH3.
有机物Ⅱ的结构简式为CH3C≡CCH=CHCH2CH3;A、B可以发生类似①的反应生成有机物Ⅰ,则该反应的化学方程式为CH3C≡CH+CH3CH2CHO$\stackrel{催化剂}{→}$CH3C≡CCH(OH)CH2CH2CH3.查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 1mol CPAE与足量的NaOH溶液反应,最多消耗3mol NaOH | |
| B. | 咖啡酸可发生聚合反应,而且其分子中含有3种官能团 | |
| C. | 与苯乙醇互为同分异构体的酚类物质共有9种 | |
| D. | 可用金属Na检测上述反应是否残留苯乙醇 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 元素 | X | Y | Z | W |
| 原子半径/nm | 0.102 | 0.16 | 0.074 | 0.071 |
| 最高正价或最低负价 | +6 | +2 | -2 | -1 |
| A. | 原子序数X>Y>W>Z | B. | 纯净的X与纯净的Z反应生成XZ3 | ||
| C. | Z的最高正价为+6 | D. | HZ是热稳定性最强的氢化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com