
分析 (1)该水的摩尔质量是22g/mol,11.0g该水的物质的量=$\frac{11.0g}{22g/mol}$=0.5mol,每个水分子中含有12个,根据N=nNA及分子构成计算中子数;每个水分子中含有2个H原子,所以该水分子中H原子物质的量=0.5mol×2=1mol,根据H原子个数相等计算甲烷物质的量;
(2)根据化学式知,n(Na2R)=$\frac{1}{2}$n(Na+)=$\frac{1}{2}$×0.4mol=0.2mol,根据M=$\frac{m}{n}$计算Na2R的摩尔质量.
解答 解:(1)该水的摩尔质量是22g/mol,11.0g该水的物质的量=$\frac{11.0g}{22g/mol}$=0.5mol,每个水分子中含有12个,水分子个数N=nNA=0.5mol×NA/mol=0.5NA,结合水分子构成知,水中中子数为6NA;每个水分子中含有2个H原子,所以该水分子中H原子物质的量=0.5mol×2=1mol,根据H原子个数相等得甲烷物质的量=$\frac{1mol}{4}$=0.25mol,故答案为:6NA;O.25;
(2)根据化学式知,n(Na2R)=$\frac{1}{2}$n(Na+)=$\frac{1}{2}$×0.4mol=0.2mol,M(Na2R)=$\frac{m}{n}$=$\frac{12.4g}{0.2mol}$=62g/mol,
故答案为:62g/mol.
点评 本题考查物质的量有关计算,为高频考点,明确物质的量公式中各个物理量关系及分子构成是解本题关键,注意(1)中水的摩尔质量不是18g/mol,为易错点.


科目:高中化学 来源: 题型:解答题
| T/K | 298 | 398 | 498 |
| 平衡常数K | 4.1×106 | K1 | K2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
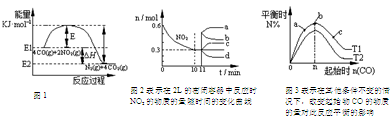
| A. | 在一定温度、固定容积的密闭容器里,混合气体的密度不再改变可以说明上述可逆反应已达平衡 | |
| B. | 由图1可得加入适当的催化剂,E减小,△H 增大 | |
| C. | 图3中T1和T2表示温度,对应温度下的平衡常数为K1、K2,则:T1<T2,K1<K2 | |
| D. | 图2中0~10min内该反应的平均速率v(CO)=0.03mol•L-1•min-1,从11min起其它条件不变,压缩容器的体积为1L,则n(NO2)的变化曲线为d |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 25℃时,有c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示.下列有关溶液中离子浓度关系的叙述正确的是( )
25℃时,有c(CH3COOH)+c(CH3COO-)=0.1mol•L-1的一组醋酸、醋酸钠混合溶液,溶液中c(CH3COOH)、c(CH3COO-)与pH 的关系如图所示.下列有关溶液中离子浓度关系的叙述正确的是( )| A. | Y点所表示的溶液中:c(CH3COO-)>c(CH3COOH)>c(H+)>c(OH-) | |
| B. | W点所表示的溶液中:c(Na+)+c(H+)+c(OH-)+c(CH3COOH)=0.1mol•L-1 | |
| C. | 该温度下醋酸的电离平衡常数为10-1 mol•L-1 | |
| D. | 向X点所表示的溶液中加入等体积的0.05 mol•L-1 NaOH溶液:c(H+)=c(CH3COOH)+c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将人群向高处疏散 | |
| B. | 将人群向顺风方向疏散 | |
| C. | 用浸有水或肥皂水(弱碱性)的毛巾捂住口鼻 | |
| D. | 向泄漏地点撒一些石灰 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用50mL的量筒量取45.50mL的水 | |
| B. | 将40gNaOH溶解于1L水中配得1mol/L的溶液 | |
| C. | CCl4萃取碘水的实验中,分液时,水层液体从下口流出 | |
| D. | 稀释浓硫酸时,把浓硫酸沿器壁慢慢注入水里,并不断搅拌 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 浓硝酸保存在带有玻璃塞的棕色试剂瓶中 | |
| B. | 已经完成定容的500mL 1.0mol•L-1的NaOH溶液,某同学不慎将容量瓶中溶液洒出部分,继续加水至溶液凹液面与刻线相切 | |
| C. | 用托盘天平称量出12.50g的NaCl固体 | |
| D. | 物质溶于水的过程中,一般有放热或吸热现象,因此溶解的操作不能在量筒中进行 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、Cl-、NO${\;}_{3}^{-}$、Ag+ | B. | H+、HCO${\;}_{3}^{-}$、Na+、Cl- | ||
| C. | Na+、OH-、Ca2+、CO${\;}_{3}^{2-}$ | D. | Mg2+、Cl-、H+、SO${\;}_{4}^{2-}$ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com