
【题目】金属磷化物(如璘化锌)是常用的蒸杀虫剂。我国卫生部门规定:粮食中化物(以PH3计)的含量不超过0.050mg:kg-1时,粮食质量方达标。现设计测定粮食中残留磷化物含量的实验如下
(资料查阅)磷化锌易水解产生PH3;PH3沸点为-88℃,有剧毒性、强还原性、易自然。
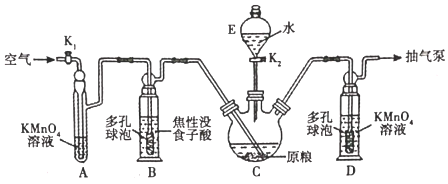
(用量标准]如图:装置A、B、E中盛有的试剂均足量;C中装有100原粮;D中盛有40.00mL6.0×10-5molL-1KMnO4溶液(H2SO4酸化)。
(操作流程)安装仪器并检査气密性→PH、的产生与吸收一转移KMnO4吸收溶液→用Na2SO3标准溶液滴定。
试回答下列问题:
(1)仪器E的名称是______;仪器B、D中进气管下端设计成多孔球泡形状,目的是______。
(2)A装置的作用是______;B装置的作用是吸收空气中的O2,防止______。
(3)下列操作中,不利于精确測定出实验结果的是______(选填序号)。
a.实验前,将C中原粮预先磨碎成粉末
b.将蒸馏水预先煮沸、迅速冷却并注入E中
c.实验过程中,用抽气泵尽可能加快抽气速率
(4)弹化锌发生水解反应时除产生PH3外,还生成______(填化学式)。
(5)D中PH3被氧化成H3PO4,该反应的离子方程式为______。
(6)把D中吸收液转移至容量瓶中,加水稀释至250.00mL,取25.00mL于锥形瓶中,用5.0×10-5molL-1的Na2SO3标准溶液滴定剩余的KMnO4溶液,消耗Na2SO3标准溶液10.00mL.则该原粮中磷化物(以PH3计)的含量为______mgkg-1,该原粮质量______(填“达标”或“不达标“)。
【答案】分液漏斗 增大接触面积 吸收空气中的还原性气体 PH3被氧化 c Zn(OH)2 5PH3+8MnO4-+24H+=5H3PO4+8Mn2++12H2O 0.085 不达标
【解析】
由实验装置图可知,实验的流程为安装吸收装置→PH3的产生与吸收→转移KMnO4吸收溶液→亚硫酸钠标准溶液滴定。已知C中盛有100g原粮,E中盛有20.00mL1.13×10-3molL-1KMnO4溶液(H2SO4酸化),吸收生成的PH3,B中盛装焦性没食子酸的碱性溶液,其作用是吸收空气中的O2,防止氧化装置C中生成的PH3,A中盛装KMnO4溶液的作用除去空气中的还原性气体。
(1)仪器E的名称是分液漏斗;仪器B、D中进气管下端设计成多孔球泡形状,目的是增大接触面积,故答案为:分液漏斗;增大接触面积;
(2)A装置的作用是吸收空气中的还原性气体;B装置的作用是吸收空气中的O2,防止PH3被氧化,故答案为:吸收空气中的还原性气体;PH3被氧化;
(3)实验前,将C中原粮预先磨碎成粉末及将蒸馏水预先煮沸、迅速冷却并注入E中,均可准确测定含量,只有实验过程中,用抽气泵尽可能加快抽气速率,导致气体来不及反应,测定不准确,故答案为:c;
(4)磷化锌易水解产生PH3,还生成Zn(OH)2,故答案为:Zn(OH)2;
(5)D中PH3被氧化成H3PO4,该反应的离子方程式为5PH3+8MnO4-+24H+=5H3PO4+8Mn2++12H2O,故答案为:5PH3+8MnO4-+24H+=5H3PO4+8Mn2++12H2O;
(6)由2KMnO4+5Na2SO3+3H2SO4=2MnSO4+K2SO4+5Na2SO4+3H2O,剩余高锰酸钾为5.0×10-5molL-1×0.01L×![]() ×
×![]() =2×10-6mol,由5PH3+8KMnO4+12H2SO4=5H3PO4+8MnSO4+4K2SO4+12H2O可知,PH3的物质的量为(0.04L×6.0×10-5molL-1-2×10-6mol)×
=2×10-6mol,由5PH3+8KMnO4+12H2SO4=5H3PO4+8MnSO4+4K2SO4+12H2O可知,PH3的物质的量为(0.04L×6.0×10-5molL-1-2×10-6mol)×![]() =2.5×10-7mol,该原粮中磷化物(以PH3计)的含量为
=2.5×10-7mol,该原粮中磷化物(以PH3计)的含量为![]() =0.08 mg/kg>0.050mg/kg,则不达标,故答案为:0.085;不达标。
=0.08 mg/kg>0.050mg/kg,则不达标,故答案为:0.085;不达标。


科目:高中化学 来源: 题型:
【题目】已知MnO2为黑色难溶于水的固体,实验室制取氧气的反应为2KClO3![]() 2KCl+3O2↑,反应后从剩余固体中回收二氧化锰的操作顺序正确的是( )
2KCl+3O2↑,反应后从剩余固体中回收二氧化锰的操作顺序正确的是( )
A. 溶解、过滤、蒸发、洗涤 B. 溶解、过滤、洗涤、加热
C. 溶解、蒸发、洗涤、过滤 D. 溶解、洗涤、过滤、加热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中含有2种官能团
B. 可与乙醇、乙酸反应,且反应类型相同
C. 1mol分枝酸最多可与3molNaOH发生中和反应
D. 可使溴的四氯化碳溶液、酸性高锰酸钾溶液褪色,且原理相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氰基丙烯酸酯在碱性条件下能快速聚合为 从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:
从而具有胶黏性。某种氰基丙烯酸酯(G)的合成路线如下:

已知:
①A的相对分子质量为58,氧元素质量分数为0.276,核磁共振氢谱显示为单峰
②
回答下列问题:
(1)A 的化学名称为__________________,。
(2)B的结构简式为____________________。其核磁共振氢谱显示为______组峰,峰面积比为_______。
(3)由C生成D的反应类型为_____________。
(4)由D生成E的化学方程式为__________________________________________________________。
(5)G中的官能团有__________、__________、__________。(填官能团名称)
(6)G的同分异构体中,与G具有相同官能团且能发生银镜反应的共有___________种。(不含立体结构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温下溶度积常数:Ksp[Pb(OH)2]=2×10-15,Ksp[Fe(OH)2]=8×10-15。当溶液中金属离子浓度小于10-5molL-1视为沉淀完全。向20mL含0.10molL-1Ph2+和0.10molL-1Fe2+的混合溶液中滴加010amolL-1NaOH溶液,金属阳离子浓度与滴入NaOH溶液体积的关系曲线如图所示,则下列说法正确的是( )
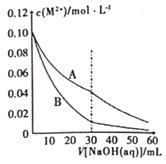
A. 曲线A表示![]() 的曲线
的曲线
B. 当溶液![]() 时,
时,![]() 开始沉淀,
开始沉淀,![]() 沉淀完全
沉淀完全
C. 滴入NaOH溶液体积大于30mL时,溶液中![]()
D. 室温下,滴加NaOH溶液过程中,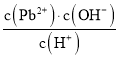 比值不断增大
比值不断增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Q、R、X、Y、Z为前20号元素中的五种,Q的低价氧化物与X单质分子的电子总数相等,R与Q同族,Y和Z的离子与Ar原子的电子结构相同且Y的原子序数小于Z。
(1)Q的最高价氧化物,其固态属于 晶体,俗名叫 ;
(2)R的氢化物分子的空间构型是 ,属于 分子(填“极性”或“非极性”);它与X形成的化合物可作为一种重要的陶瓷材料,其化学式是 ;
(3)X的常见氢化物的空间构型是 ,它的另一氢化物X2H4是一种火箭燃料的成分,其电子式是 ;
(4)Q分别与Y、Z形成的共价化合物的化学式是 和 ,Q与Y形成的分子的电子式是 ,属于 分子(填“极性”或“非极性”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面的排序不正确的是
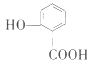
A. 晶体的熔点:![]() >
>
B. 晶格能的大小: Al2O3>MgCl2>NaCl
C. 共价键的键长: F-F>C-Cl>C-S>Si-O
D. 硬度由大到小:金刚石>氮化硅>晶体硅
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A.由Na2CO3 + SiO2 ![]() Na2SiO3 + CO2↑可知,酸性H2SiO3>H2CO3
Na2SiO3 + CO2↑可知,酸性H2SiO3>H2CO3
B.氢氟酸需要密封存放在橡胶塞的玻璃试剂瓶中
C.向硅酸钠溶液中加入盐酸产生白色沉淀,过量时沉淀溶解
D.瓷坩埚、氧化铝坩埚均不可作为融化NaOH固体的装置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】研究铜和铁与浓硫酸的反应,实验如下:
① | ② |
| |
铜丝表面无明显现象 铁丝表面迅速变黑,之后无明显现象 | 铜丝或铁丝逐渐溶解,产生大量气体, 品红溶液褪色 |
下列说法正确的是
A. 常温下不能用铁制容器盛放浓硫酸,可用铜制容器盛放浓硫酸
B. ②中铜丝或铁丝均有剩余时,产生气体的物质的量相等
C. 依据②,可推断出铜和铁与浓硫酸反应可生成SO2
D. ①②中现象的差异仅是由于温度改变了化学反应速率
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com