
【题目】下列说法正确的是![]()
A.金属钠和其他碱金属都可保存在煤油中
B.湿法冶炼是指金属在溶液中发生的置换反应,如金属钠置换出硫酸铜溶液中的铜
C.用铂丝蘸取少量某溶液进行焰色反应,火焰呈黄色,该溶液一定是钠盐溶液
D.制备![]() 、
、![]() 、
、![]() 均不能采用将溶液直接蒸干的方法
均不能采用将溶液直接蒸干的方法
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.相同物质的量浓度的下列溶液中,①NH4Al(SO4)2、②NH4Cl、③CH3COONH4、④NH3·H2O; c(NH4+) 由大到小的顺序是:①>②>③>④
B.某物质的溶液中由水电离出的c(H+)=1×10-a mol/L,若a>7时,则该溶液的pH一定为14-a
C.物质的量浓度相等的H2S和NaHS混合溶液中:c(Na+) +c(H+) =c(S2―) +c (HS―)+c (OH―)
D.AgCl悬浊液中存在平衡: AgCl(s)![]() Ag+(aq)+Cl―(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
Ag+(aq)+Cl―(aq),往其中加入少量 NaCl粉末,平衡会向左移动,溶液中离子的总浓度会减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一绝热容积不变的密闭容器中发生可逆反应![]() ,以下不能说明该反应达到化学平衡状态的是( )
,以下不能说明该反应达到化学平衡状态的是( )
A.混合气体的密度不再变化B.v逆(X)=v正(Y)
C.X、Y的浓度比为1:1D.体系压强不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置,若开始时a、b两端液面相平,放置一段时间后,下列有关叙述中正确的是( )
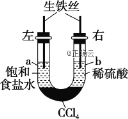
A.铁丝在两处的腐蚀速率:a>b
B.a、b两端相同的电极反应式为![]()
C.一段时间后,a端液面高于b端液面
D.a处总反应为:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】环境问题已成为人类共同关注的话题,燃煤废气、汽车尾气中常含有的NOx、SO2、H2S等污染物,容易形成酸雨,破坏环境。其综合治理是当前重要的研究课题。
Ⅰ.以下是对酸雨的若干项评价,其中不正确的是__________
a.杀死水中的浮游生物,减少鱼类食物的来源,破坏水生生态系统
b.对电线、铁轨、桥梁、房屋等均会造成严重损害
c.导致臭氧层空洞
d.二氧化碳的过量排放,是形成酸雨的主要原因之一
Ⅱ.电解法处理氮氧化物废气有较高的环境效益和经济效益(图中电极均为石墨)。

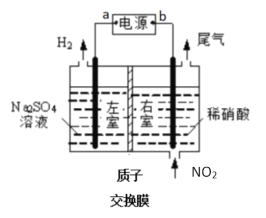
(1)电解NO制备NH4NO3原理如上方左图所示:
①阳极为石墨_____(填1或2),该电极的反应式为_____________。
②为使电解的副产物也完全转化为NH4NO3,需要补充的物质X的化学式为___________。
(2)用上方右图装置进行模拟电解NO2气体实验,可回收硝酸。
①外接电源a极为______极,左室发生的电极反应式为_____________。
②若有标准状况下2.24L NO2被吸收,通过质子交换膜(只允许质子通过)的H+为______mol。
③用含NO和NO2(不考虑NO2转化为N2O4)的废气进行模拟电解法吸收实验。电解过程中,有部分NO转化为HNO2。实验结束时,测得右室溶液中增加了1 mol HNO3、0.1 mol HNO2,同时左室收集到标准状况下28L H2。原气体中NO和NO2的体积比为____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组混合物的总物质的量一定,每组中的物质以任意比例相混合,完全燃烧时消耗氧气的量不变的是
A.甲烷、甲醇和甲醛B.甲醇、甲醛和甲酸
C.乙醇、乙烯和丙烯酸D.甲酸、乙二酸和乙二醇
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙酰紫草素具有抗菌、抗炎、抗病毒、抗肿瘤等作用,它的结构简式如图所示,下列有关乙酰紫草素的说法正确的是

A. 该分子中含有1个手性碳原子
B. 1mol乙酰紫草素最多可与2mol NaOH反应
C. 1mol 乙酰紫草素最多可与2mol Br2反应
D. 能与FeCl3溶液发生显色反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池能长时间保持稳定的放电电压。高铁电池的总反应为:3Zn+2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+4KOH,下列叙述不正确的是( )
A.放电时负极反应为:Zn-2e-+2OH-=Zn(OH)2
B.充电时阳极反应为:Fe(OH)3-3e-+5OH-=FeO42-+4H2O
C.充电时,蓄电池的负极应与外接电源正极相连
D.放电时负极附近溶液的碱性减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知室温时,0.1mo1/L某一元酸HA在水中有0.1%发生电离,下列叙述错误的是:
A. 该溶液的pH=4 B. 升高温度,溶液的pH增大 C. 此酸的电离平衡常数约为1×10-7 D. 由HA电离出的c(H+)约为水电离出的c(H+)的106倍
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com