
| A | ||
| C | B |
| A、A元素的最高正价为+6价 |
| B、A、B、C依次是氧、氯、磷 |
| C、B元素的单质常温下是一种黄绿色气体 |
| D、C单质常用来制作计算机的芯片 |


 通城学典默写能手系列答案
通城学典默写能手系列答案科目:高中化学 来源: 题型:
 瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图所示,有关说法正确的是( )
瑞典ASES公司设计的曾用于驱动潜艇的液氨-液氧燃料电池示意图如图所示,有关说法正确的是( )| A、电极2发生氧化反应 |
| B、电池工作时,Na+向负极移动 |
| C、电流由电极1经外电路流向电极2 |
| D、电极1发生的电极反应为:2NH3+6OH--6e-=N2↑+6H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
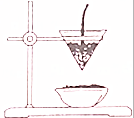 下图为教材铝热反应演示实验示意图
下图为教材铝热反应演示实验示意图查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1.5mL | B、2.4mL |
| C、3.6mL | D、4mL |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| 1 |
| 2 |
| 1 |
| 2 |
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①②③ | B、①②④ |
| C、②③⑤ | D、③④⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com