

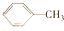
 $\stackrel{KMnO_{4}(H)}{→}$
$\stackrel{KMnO_{4}(H)}{→}$
 $\stackrel{一定条件}{→}$
$\stackrel{一定条件}{→}$  (苯胺,弱碱性,易氧化)
(苯胺,弱碱性,易氧化)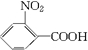 .
. .
. .
.分析 甲苯在光照条件发生甲基上取代反应生成 ,由A系列反应得到E,反应中引入-COOH、-NH2,且处于邻位,甲基氧化得到-COOH,由题目信息可知,-NO2还原得到-NH2,由于苯胺易被氧化,所以用KMnO4(H+)先氧化-CH3成-COOH,再将-NO2还原得到-NH2,故A转化得到B是甲苯的硝化反应,可知B为
,由A系列反应得到E,反应中引入-COOH、-NH2,且处于邻位,甲基氧化得到-COOH,由题目信息可知,-NO2还原得到-NH2,由于苯胺易被氧化,所以用KMnO4(H+)先氧化-CH3成-COOH,再将-NO2还原得到-NH2,故A转化得到B是甲苯的硝化反应,可知B为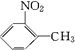 ,C为
,C为 ,D和E发生取代反应,由信息Ⅰ可知生成F为
,D和E发生取代反应,由信息Ⅰ可知生成F为 ,据此解答.
,据此解答.
解答 解:甲苯在光照条件发生甲基上取代反应生成 ,由A系列反应得到E,反应中引入-COOH、-NH2,且处于邻位,甲基氧化得到-COOH,由题目信息可知,-NO2还原得到-NH2,由于苯胺易被氧化,所以用KMnO4(H+)先氧化-CH3成-COOH,再将-NO2还原得到-NH2,故A转化得到B是甲苯的硝化反应,可知B为
,由A系列反应得到E,反应中引入-COOH、-NH2,且处于邻位,甲基氧化得到-COOH,由题目信息可知,-NO2还原得到-NH2,由于苯胺易被氧化,所以用KMnO4(H+)先氧化-CH3成-COOH,再将-NO2还原得到-NH2,故A转化得到B是甲苯的硝化反应,可知B为 ,C为
,C为 ,D和E发生取代反应,由信息Ⅰ可知生成F为
,D和E发生取代反应,由信息Ⅰ可知生成F为 ,
,
(1)由上述分析可知,C的结构简式是 ,
,
故答案为: ;
;
(2)反应②的化学方程式为 ,
,
故答案为: ;
;
(3)反应⑤的化学方程式为 ,
,
故答案为: ;
;
(4)反应①属于取代反应,反应②属于取代反应,反应③属于氧化反应,反应④属于还原反应,反应⑤属于取代反应,
故答案为:①②⑤.
点评 本题考查有机物的推断与合成,根据题目信息结合有机物的结构判断发生的反应,进而推断其它物质的结构简式,注意掌握有机物官能团的性质与转化,难度中等.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 盐酸、空气、醋酸、干冰 | B. | 铁、海水、硫酸钠、乙醇 | ||
| C. | 硫酸、蔗糖、烧碱、石灰石 | D. | 胆矾、漂白粉、氯化钾、硫酸钡 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分液时,分液漏斗中下层液体从下口放出,上层液体上口倒出 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还需加少量蒸馏水再趁热过滤 | |
| D. | 除去混在乙酸乙酯中杂质乙酸时,可先加入饱和烧碱溶液振荡后静置,再分液 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯的球棍模型为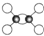 | |
| B. | H2O2的电子式为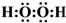 | |
| C. | 甲烷的结构式为CH4 | |
| D. | 乙酸乙酯的结构简式为CH3COOCH3CH2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯(硝基苯):加少量蒸馏水振荡,待分层后分液 | |
| B. | CO2(HCl、水蒸气):通过盛有碱石灰的干燥管 | |
| C. | 乙烷(乙烯):通入氢气发生加成反应 | |
| D. | 乙醇(水):加新制的生石灰,蒸馏 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe Cu Al Ag Mg | B. | Al Cu Mg Ag Fe | ||
| C. | Mg Cu Al Ag Fe | D. | Mg Ag Al Cu Fe |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
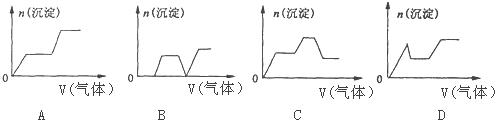
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cl-Cl键比H-H键的键能小,是因为Cl原子比H原子的非金属性强 | |
| B. | H2(g)与Cl2(g)反应生成2 molHCl(g),反应的△H=183 kJ/mol | |
| C. | H2(g)与Cl2(g)反应生成2 molHCl(g),反应的△H=-183 kJ/mol | |
| D. | H2(g)与Cl2(g)反应生成1 molHCl(g),反应的△H=-183 kJ/mol |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com