


科目:高中化学 来源: 题型:
 向盛有氯气的集气瓶中,注入约五分之一的下列液体并轻轻振荡,观察到的现象记录如图所示,判断瓶中注入的液体是( )
向盛有氯气的集气瓶中,注入约五分之一的下列液体并轻轻振荡,观察到的现象记录如图所示,判断瓶中注入的液体是( )| A、AgNO3溶液 |
| B、NaOH溶液 |
| C、水 |
| D、FeCl2溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在任何条件下,化学平衡常数K都是一个定值 |
| B、当改变反应物的浓度时,化学平衡常数会发生改变 |
| C、化学平衡常数K只与温度有关,与反应物浓度、体系的压强无关 |
| D、化学平衡常数K与反应物的转化率是一一对应的 |
查看答案和解析>>
科目:高中化学 来源: 题型:
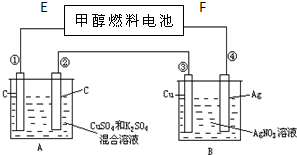 如图所示,用甲醇和氧气以及强碱做电解质溶液的新型燃料电池做电源,对A、B 装置通电一段时间后,发现有1.6g甲醇参加反应且③电极增重(假设工作时无能量损失).请回答下列问题:
如图所示,用甲醇和氧气以及强碱做电解质溶液的新型燃料电池做电源,对A、B 装置通电一段时间后,发现有1.6g甲醇参加反应且③电极增重(假设工作时无能量损失).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、△H>0,△S>0 |
| B、△H>0,△S<0 |
| C、△H<0,△S>0 |
| D、△H<0,△S<0 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 能使酸性高锰酸钾溶液褪色 |
B、 中的碳碳键是介于碳碳叁键和碳碳双键之间的独特的键 |
C、 可与溴水发生加成反应使溴水褪色 |
D、 在稀硫酸作用下可与乙酸发生取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
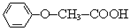 )发生酯化反应的产物.
)发生酯化反应的产物.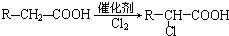 ,R-ONa
,R-ONa| Cl-R′ |
| △ |
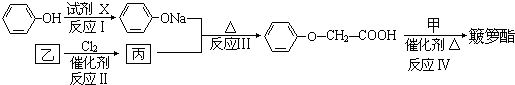
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com