
下列指定反应的离子方程式正确的是( )
A.Cu溶于稀HNO3:Cu+2H++NO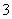 ===Cu2++NO2↑+H2O
===Cu2++NO2↑+H2O
B.(NH4)2Fe(SO4)2溶液与过量NaOH溶液反应制Fe(OH)2:Fe2++2OH-===Fe(OH)2↓
C.用CH3COOH溶解CaCO3:CaCO3+2H+===Ca2++H2O+CO2↑
D.向NaAlO2溶液中通入过量CO2制Al(OH)3:CO2+AlO +2H2O===Al(OH)3↓+HCO
+2H2O===Al(OH)3↓+HCO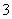
科目:高中化学 来源: 题型:
有一种酸式盐AHB,它的水溶液呈弱碱性。则以下说法中错误的是( )
A.相同物质的量浓度的AOH溶液和H2B溶液,前者的电离程度大于后者的电离程度;
B.H2B不是强酸;
C.HB-的电离程度大于HB-的水解程度;
D.该盐溶液的电离方程式一般写成:AHB??A++HB-,HB-??H++B2-
查看答案和解析>>
科目:高中化学 来源: 题型:
判断正误,正确的划“√”,错误的划“×”
(1)强电解质溶液的导电性比弱电解质溶液的导电性强( )
(2)BaSO4投入水中, 导电性较弱,故它是弱电解质( )
(3)弱电解质溶液中存在两种共价化合物分子( )
(4)强电解质都是离子化合物,弱电解质都是共价化合物( )
(5)CaO是强电解质,是因为它的水溶液能导电( )
(6)Cl2的水溶液能导电,所以Cl2是电解质( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列解释事实的方程式不正确的是( )
A.测0.1 mol·L-1氨水的pH为11:NH3·H2O??NH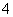 +OH-
+OH-
B.将Na块放入水中,产生气体:2Na+2H2O===2NaOH+H2↑
C.用CuCl2溶液做导电实验,灯泡发光:CuCl2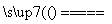 Cu2++2Cl-
Cu2++2Cl-
D.Al片溶于NaOH溶液中,产生气体:2Al+2OH-+2H2O===2AlO +3H2↑
+3H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在水溶液中的电离方程式错误的是( )
A.NaHCO3===Na++H++CO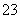
B.NaHSO4===Na++H++SO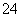
C.MgCl2===Mg2++2Cl-
D.Ba(OH)2===Ba2++2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
由CH3CH2CH2Br制备CH3CH(OH)CH2OH,依次(从左至右)发生的反应类型和反应条件都正确的是( )
| 选项 | 反应类型 | 反应条件 |
| A | 加成反应、取代反应、消去反应 | KOH醇溶液/加热、KOH水溶液/加热、常温 |
| B | 消去反应、加成反应、取代反应 | NaOH醇溶液/加热、常温、NaOH水溶液/加热 |
| C | 氧化反应、取代反应、消去反应 | 加热、KOH醇溶液/加热、KOH水溶液/加热 |
| D | 消去反应、加成反应、水解反应 | NaOH水溶液/加热、常温、NaOH醇溶液/加热 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com