
【题目】碳和碳的化合物广泛的存在于我们的生活中。
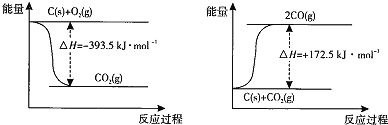
(1)根据下列反应的能量变化示意图,![]() ______ 。
______ 。
(2)在体积为2L的密闭容器中,充入1mol ![]() 和3mol H,一定条件下发生反应:
和3mol H,一定条件下发生反应:![]() ,测得
,测得![]() 和
和![]() 的物质的量随时间变化的曲线如图所示:
的物质的量随时间变化的曲线如图所示:

①从反应开始到平衡,![]() 的平均反应速率
的平均反应速率![]() ______ 。
______ 。
②下列措施中能使化学平衡向正反应方向移动的是 ______ ![]() 填编号
填编号![]() 。
。
A.升高温度
![]() 将
将![]() 及时液化移出
及时液化移出
C.选择高效催化剂
![]() 再充入1mol
再充入1mol ![]() 和4mol
和4mol ![]()
(3)![]() 溶于水生成碳酸。已知下列数据:
溶于水生成碳酸。已知下列数据:
弱电解质 |
|
|
电离平衡常数 |
|
|
现有常温下![]() 的
的![]() 溶液,已知:
溶液,已知:![]() 水解的平衡常数
水解的平衡常数![]() ,
,![]() 第一步水解的平衡常数
第一步水解的平衡常数![]() 。
。
①判断该溶液呈 ______ ![]() 填“酸”、“中”、“碱”
填“酸”、“中”、“碱”![]() 性,写出该溶液中
性,写出该溶液中![]() 发生第一步水解的离子方程式 ______ 。
发生第一步水解的离子方程式 ______ 。
②下列粒子之间的关系式,其中正确的是 ______ 。
A.![]()
B.![]()
C.![]()
D.![]()
(4)据报道,科学家在实验室已研制出在燃料电池的反应容器中,利用特殊电极材料以CO和![]() 为原料做成电池。原理如图所示:
为原料做成电池。原理如图所示:
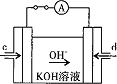
通入CO的管口是 ______ ![]() 填“c”或“d”
填“c”或“d”![]() ,写出该电极的电极反应式: ______ 。
,写出该电极的电极反应式: ______ 。
【答案】![]()
![]() BD 碱
BD 碱 ![]() CD
CD ![]()
![]()
【解析】
(1)先根据图象写出对应的化学方程式,然后根据盖斯定律来解答;
(2)①根据反应速率![]() 计算v(CH3OH),再根据速率之比等于化学计量数之比计算v(H2O);
计算v(CH3OH),再根据速率之比等于化学计量数之比计算v(H2O);
②根据平衡移动原理解答,改变影响平衡的一个条件(如浓度、压强或温度等),平衡就向能够减弱这种改变的方向移动;
(3)①根据CO32-第一步水解的平衡常数大于NH4+水解的平衡常数可知溶液呈碱性;碳酸根离子分步水解,第一步水解水解生成氢氧根离子和碳酸氢根离子;
②根据电荷守恒、物料守恒和质子守恒分析;
(4)先根据原电池中阴离子流向负极,确定正负极,然后根据燃料电池中燃料作还原剂,在负极失去电子发生氧化反应;
(1)由左图得到:![]()
由右图得到:![]()
![]()
根据盖斯定律,由![]() 得:
得:![]() ;
;
故答案为:![]() ;
;
(2)![]() 从反应开始到平衡,
从反应开始到平衡, ,速率之比等于化学计量数之比,故
,速率之比等于化学计量数之比,故![]() ;故答案为:
;故答案为:![]() ;
;
![]() A.升高温度,平衡向吸热的方向移动,而该反应正反应放热,所以反应逆向移动,故A错误;
A.升高温度,平衡向吸热的方向移动,而该反应正反应放热,所以反应逆向移动,故A错误;
B.将![]() 及时液化移出,生成物的浓度减少,平衡正向移动,故B正确;
及时液化移出,生成物的浓度减少,平衡正向移动,故B正确;
C.选择高效催化剂,化学反应速率加快,但平衡不移动,故C错误;
D.再充入![]() 和
和![]() ,反应物浓度增大,平衡正向移动,故D正确;
,反应物浓度增大,平衡正向移动,故D正确;
故选BD;
(3)![]() 第一步水解的平衡常数
第一步水解的平衡常数![]() 大于
大于![]() 水解的平衡常数
水解的平衡常数![]() ,可知溶液呈碱性;碳酸根离子分步水解,第一步水解水解生成氢氧根离子和碳酸氢根离子,其水解方程式为:
,可知溶液呈碱性;碳酸根离子分步水解,第一步水解水解生成氢氧根离子和碳酸氢根离子,其水解方程式为:![]() ;故答案为:碱;
;故答案为:碱;![]() ;
;
![]() 溶液中铵根离子浓度大于碳酸根离子浓度,碳酸根离子水解程度大于铵根离子水解程度,所以溶液中离子浓度大小为:
溶液中铵根离子浓度大于碳酸根离子浓度,碳酸根离子水解程度大于铵根离子水解程度,所以溶液中离子浓度大小为:![]() ,故A错误;
,故A错误;
B.溶液中存在电荷守恒为:![]() ,故B错误;
,故B错误;
C.依据溶液中物料守恒得到:![]() ,故C正确;
,故C正确;
D.依据溶液中物料守恒,![]() :
:![]() :1,结合溶液中离子种类和守恒关系得到:
:1,结合溶液中离子种类和守恒关系得到:![]() ,故D正确;
,故D正确;
故答案为:CD;
(4)由图可知,氢氧根离子流向负极,则d为负极,e为正极,燃料电池中CO作还原剂,在负极发生反应,电极反应为:![]() ,所以通入CO的管口是d。故答案为:d;
,所以通入CO的管口是d。故答案为:d;![]() 。
。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】25℃时,将0.1 mol/L的NaOH溶液滴入盛有50 mLpH=2 的HA溶液的绝热容器中,加入NaOH溶液的体积V与溶液温度T的关系如图。下列说法正确的是( )

A.a点溶液中,c(A-)+c(HA)=0.08 mol/L
B.b点溶液中,c(A-)<c(Na+)
C.a→b的过程中,发生了吸热反应
D.溶液中HA的电离平衡常数a点等于b点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,发生反应:①M(s)+N(g) ![]() R(g) △H=—Q1 kJ/mol,②2R(g)+N(g)
R(g) △H=—Q1 kJ/mol,②2R(g)+N(g) ![]() 2T(g) △H=—Q2 kJ/mol.Q1、Q2、Q3均为正值.下列说法正确的是 ( )
2T(g) △H=—Q2 kJ/mol.Q1、Q2、Q3均为正值.下列说法正确的是 ( )
A.1mol R(g)的能量总和大于1mol M(s)与1mol N(g)的能量总和
B.将2mol R(g)与1mol N(g)在该条件下反应,可以放出热量Q2 kJ
C.当1mol M(s)完全转化为T(g)时(假定无热量损失),放出热量![]()
D.M(g)+N(g) ![]() R(g) △H=—Q3 kJ/mol,则Q3 >Q1
R(g) △H=—Q3 kJ/mol,则Q3 >Q1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原滴定同中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。现用0.0010 mol·L1酸性KMnO4溶液滴定未知浓度的无色NaHSO3溶液,反应的离子方程式为2![]() +5
+5![]() +H+=2Mn2++5
+H+=2Mn2++5![]() +3H2O。请完成下列问题:
+3H2O。请完成下列问题:
(1)该实验除了滴定管(50 mL)、铁架台、滴定管夹、烧杯 、白纸等仪器和用品外,还必须使用的仪器是____________。
(2)实验中用_____(填“酸”或“碱”)式滴定管盛装酸性KMnO4溶液,原因是_______。
(3)本实验_______(填“需要”或“不需要”)使用指示剂,滴定终点的现象是__________。
(4)①滴定前平视液面,刻度为a mL,滴定后俯视刻度为b mL,根据(ba) mL计算得到的待测液浓度比实际浓度_____(填“高”或“低”)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的待测液浓度值会____(填“偏小”“偏大”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某工厂对制革工业污泥中铬的处理工艺流程如下:

已知硫酸浸取液中的金属离子主要是Cr3+,其次是Fe3+、Al3+、Ca2+和Mg2+。
(1)酸浸时,为了提高浸取率可采取的措施有_________、___________。(答出两点)。
(2)常温下,部分阳离子以氢氧化物形式沉淀时溶液的pH如下:
阳离子 | Fe3+ | Al3+ | Cr3+ |
开始沉淀时的pH | 2.7 | — | — |
沉淀完全时的pH | 3.7 | 5.4(>8溶解) | 9(>9溶解) |
①用NaOH调节溶液的pH不能超过8,其理由是________________________________。
②常温下,当pH=8时,Mg2+是否开始沉淀(溶液中镁离子浓度不超过1mol·L-1)___________ 。 (填“是”或“否”)若要使Mg2+完全沉淀,溶液的pH至少为_________(已知Ksp[Mg(OH)2]=1. 6×10-12,lg2=0.3)。
查看答案和解析>>
科目:高中化学 来源: 题型:
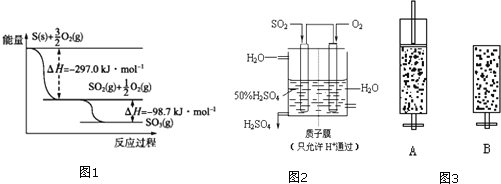
【题目】工业上利用硫黄生产硫酸的步骤及反应为:
①造气: ;
;
②催化氧化:![]() ;
;
③吸收:![]() 。
。
(1)根据图1写出![]() 与
与![]() 反应生成
反应生成![]() 的热化学方程式: ______ 。
的热化学方程式: ______ 。
(2)某温度下![]() ;
;![]() 。开始时在10L的密闭容器中加入
。开始时在10L的密闭容器中加入![]() 和
和![]() ,当反应达到平衡时共放出热量196kJ,求该温度下
,当反应达到平衡时共放出热量196kJ,求该温度下![]() 平衡常数K=______ 。
平衡常数K=______ 。
(3)某人设想以图2所示装置用电化学原理生产硫酸,写出通入![]() 的电极的电极反应式: ______ 。
的电极的电极反应式: ______ 。
(4)有两只密闭容器A和B,A容器有一移动的活塞能使容器内保持恒压,B容器能保持恒容,起始向这两只容器中分别充入等量的体积比为2:1的![]() 和
和![]() 的混合气体,并使A和B容积相等
的混合气体,并使A和B容积相等![]() 如图
如图![]() ,
,![]() 时发生如下反应:
时发生如下反应:![]() 填写下列空格:
填写下列空格:
①![]() 容器中
容器中![]() 的转化率比B容器 ______
的转化率比B容器 ______
②达到![]() 所述平衡后,若向两容器通入等量的原反应气体,达到平衡时A容器中
所述平衡后,若向两容器通入等量的原反应气体,达到平衡时A容器中![]() 的体积分数 ______
的体积分数 ______ ![]() 增大、减小、不变
增大、减小、不变![]() ,B容器中
,B容器中![]() 的体积分数 ______
的体积分数 ______ ![]() 增大、减小、不变
增大、减小、不变![]()
(5)对于反应![]() ,一定条件下达到平衡后,在保证O2浓度不变的情况下,增大容器的体积,试根据平衡常数,判断平衡 ______
,一定条件下达到平衡后,在保证O2浓度不变的情况下,增大容器的体积,试根据平衡常数,判断平衡 ______ ![]() 填“正向移动”、“逆向移动”或“不移动”
填“正向移动”、“逆向移动”或“不移动”![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图为阳离子交换膜法电解饱和食盐水原理示意图。下列说法不正确的是( )

A.粗盐水中含Ca2+、Mg2+、SO42-等离子,精制时除杂试剂BaCl2溶液应在Na2CO3溶液之前加入
B.标准状况下每生成22.4LCl2,便产生2 mol NaOH
C.从E口逸出的气体是Cl2
D.从B口加入含少量NaOH的水溶液以增强导电性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【化学——选修3:物质结构与性质】
铬、锰、铁、钴、镍等过渡金属元索的单质及其化合物在工农业、国防、科技等领域具存广泛应用。
(1)基态Cr原子中有_________个未成对电子,最外层电子所占用能级的电子云形状为_______。
(2)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关,一般地,为d0或d10排布时,无颜色;为d1d9排布时,有颜色。则:[Mn(H2O)6]2+ ________(填“无”或“有”)颜色。
(3)不同温度下,铁单质晶胞的两种堆积方式如图所示
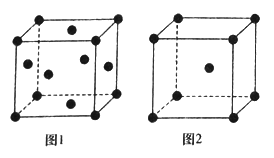
①图1和图2中Fe原子的配位数分别为_______________和________________。
②若图2的晶体密度为ρg·cm-3,阿伏加德罗常数的值为NA,则晶胞中两个最近的Fe原子之间的距离为__________pm。(用含ρ、NA的代数式表示)
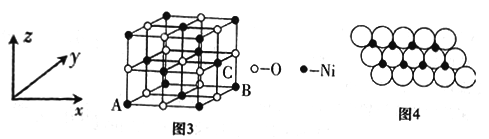
(4)已知MgO与NiO的晶体结构(如图3)相同,其中Mg2+和Ni2+的离子半径分别为66pm和69pm。则熔点:MgO__________NiO(填“>”“<”或“=”),理由是_______________。若NiO晶胞中离子坐标参数A为(0,0,0),B为(1,1,0),则C离子坐标参数为_______________。
(5)一定温度下,NiO晶体可以自发地分散并形成“单分子层”,可以认为O2-作密置单层排列,Ni2+填充其中(如图4),已知O2-的半径为ɑ m,每平方米面积上分散的该晶体的质量为_________g。(用含ɑ、NA的代数式表示)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com