
【题目】(I)某化学实验小组为确定过氧化氢分解的最佳催化条件,用如图装置进行实验,反应物用量和反应停止的时间数据如下表:

请回答下列问题:
(1)盛装双氧水的化学仪器名称是__________。
(2)如何检验该套装置的气密性__________。
(3)相同浓度的过氧化氢,其分解速率随着二氧化锰用量的增加而__________。
(4)从实验效果和“绿色化学”的角度考虑,双氧水的浓度相同时,加入______g的二氧化锰为较佳选择。
(5)某同学分析上述数据后认为:“当用相同质量的二氧化锰时,双氧水的浓度越小,所需要的时间就越少,亦即其反应速率越快”的结论,你认为是否正确_______,理由是__________。(提示:H2O2的密度可认为近似相等)。
(II)在如图所示的量热计中,将100mL0.50mol/LCH3COOH溶液与100mL0.55mol/LNaOH溶液混合。温度从25.0℃升高到27.7℃。已知量热计的热容常数(量热计各部件每升高1℃所需的热量)是150.5J/℃生成溶液的比热容为4.184J·g-1·℃-1,溶液的密度均近似为1g/mL。

(1)试求CH3COOH的中和热△H=__________。
(2)CH3COOH的中和热的文献值为56.1kJ/mol,则请你分析在(1)中测得的实验值偏差可能的原因_____________。
(3)实验中NaOH过量的目的是_____________。
【答案】 分液漏斗 加快 0.3 关闭分液潮斗活塞,将注射器的活栓向外拉出一段距离,若一段时间后活栓能够恢复到原位置,则装置的气密性好 不正确 H2O2的浓度扩大二倍(从1.5%→3.0%),但反应所需时间比其二倍小得多 -53.3kJ/mol 量热计的保温瓶绝热效果不好 酸碱溶液混合不迅速 温度计不够精确等 使碱稍稍过量,为了能保证CH3COOH溶液完全被中和,从而提高实验的准确度
【解析】试题分析:(Ⅰ)(1)根据仪器构造可知,盛装双氧水的化学仪器名称是分液漏斗;
(2)根据装置的结构特点可知,检验该装置气密性的方法是:关闭分液漏斗的活塞,将注射器的活栓向外拉出一段距离,若一段时间后活栓能够恢复到原位置,则装置的气密性好。
(3)由表中数据可知,双氧水的量相同,加入的二氧化锰质量越多,反应所需的时间越短,说明反应速率越快,故答案为:加快;
(4)根据表中数据,在双氧水的浓度相同时,加入0.3g二氧化锰与加入0.1g二氧化锰对化学反应速率影响相差较大,加入0.3g二氧化锰与加入0.5g二氧化锰对反应速率的影响相差不是很大,所以加入二氧化锰的最佳量为0.3g,故答案为:0.3;
(5)从表中数据可知,相同体积3.0%的双氧水中的溶质含量是1.5%的双氧水中溶质含量的二倍,但反应的时间却比其反应时间的二倍小得多,由反应速率计算公式(v=△c÷△t)可得出,此实验条件下双氧水的浓度越大分解速率越快。
(Ⅱ):(1)CH3COOH的中和热Q=△H=Q=-cm△T=
![]() =-5.33×104Jmol-1=-53.3 kJmol-1。
=-5.33×104Jmol-1=-53.3 kJmol-1。
(2)CH3COOH的中和热的文献值为56.1KJ· mol-1,这说明测量值偏小,这是由于醋酸是弱酸,电离吸热,也可能是①量热计的保温瓶绝热效果不好;②酸碱溶液混合不迅速;③温度计不够精确等。
(3)酸和碱反应测中和热时,为了保证一方全部反应,往往需要另一试剂稍稍过量,减少实验误差。


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均为有机物,其中A是化学实验中最常见的有机物,它易溶于水并有特殊香味;B的产量可衡量一个国家石油化工发展的水平,有关物魇的转化关系如图①所示: 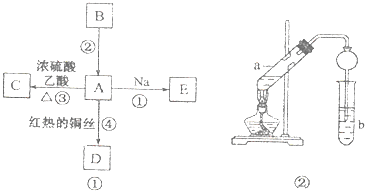
(1)A中官能团的名称为 .
(2)写出下列反应的化学方程式反应①;反应④;
(3)实验室利用反应③制取C,常用上图②装置: ①a试管中的主要化学反应的方程式为: .
②在实验中球形干燥管除起冷凝作用外,另一个重要作用是 .
③试管b中观察到的现象是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z、W在周期表中的相对位置如右图,X的氢化物能与其最高价氧化物对应的水化物反应生成盐。下列判断正确的是

A. 最简单气态氢化物的稳定性:X<Y
B. 单核阴离子的还原性:W>Z
C. 含Z元素的盐溶液可能显酸性、碱性或中性
D. Y、Z、W的含氧酸的酸性依次增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水的电离平衡曲线如图所示。下列说法中,正确的是

A. 图中A、D、E三点处KW间的关系:E处>A处>D处
B. 温度不变时,往水中通入适量HCl气体,可以使水的电离从A点变化到D点
C. 温度不变时,在水中加入适量CH3COONa固体,可以使水的电离从A点变化到C点
D. 在B点处,0.5 mol·L-1的H2SO4溶液与1 mol·L-1的KOH溶液等体积混合,充分反应后,所得溶液的pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】证明海带中含有碘元素的实验方案如下,请你按要求补充完整:
步骤 | 实验过程 | 实验用品 |
I | 将干海带灼烧灰化 |
|
II | 将海带灰溶解、过滤 |
|
III | 氧化滤液中的I﹣ , 反应的离子方程式为② |
|
IV | 取少量III中反应后溶液于试管中,加入少量CCl4并振荡后静置,观察到③ , 说明海带中含有碘元素 |
|
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com