
| A. | 盖斯定律为我们提供了解决很难由实验直接测定而获得反应热的理论依据 | |
| B. | 若用50mL 0.50mo1•L-1的氢氧化钠溶液,分别与50mL 0.50mo1•L-1的盐酸和50mL 0.25mo1•L-1的硫酸充分反应,两反应测定的反应热不相等 | |
| C. | 实验时只需要记录反应体系的最高温度t即可 | |
| D. | 酸碱混合时,量筒中NaOH溶液应缓缓倒入小烧杯中,再用环形玻璃搅拌棒不断搅拌 |
分析 A.盖斯定律可以计算反应很慢或不直接发生的反应的反应热;
B.中和热是强酸和强碱反应生成1mol水时放出的热量,与酸碱的用量无关;
C.中和热的测定中需要测量初始温度和最高温度;
D.为防止热量的散失,实验操作要迅速.
解答 解:A.有些反应很慢,有的反应不直接发生,其反应热通过实验测定有困难,可以用盖斯定律间接计算出来,故A正确;
B.中和热是强酸和强碱反应生成1mol水时放出的热量,与酸碱的用量无关,所以两反应测定的中和热相等,故B错误
C.实验时需要记录初始温度T1和最高温度T2,代入公式计算,故C错误;
D.酸碱混合时,要保证NaOH溶液的温度和酸的温度一样,在立即倒入小烧杯中和酸混合反应,故D错误;
故选A.
点评 本题考查了中和热的测定方法及其判断,题目难度不大,明确中和热的测定步骤及操作方法为解答关键,试题侧重考查学生的分析能力、理解能力及化学实验能力.


科目:高中化学 来源: 题型:选择题
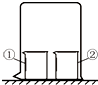 用图所示装置进行下列实验,实验结果与预测现象不一致的是( )
用图所示装置进行下列实验,实验结果与预测现象不一致的是( )| 选项 | ①中物质 | ②中物质 | 预测现象 |
| A | 酚酞溶液 | 浓氨水 | ①中无色变红色 |
| B | CCl4 | 液溴 | ①中变橙色 |
| C | 浓氨水 | 浓硫酸 | 空气中产生白烟 |
| D | NaAlO2溶液 | 浓盐酸 | ①中有白色沉淀 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在化学反应进行的过程中放出或吸收的热量称为反应热 | |
| B. | 在稀溶液中,1mol酸跟1mol碱发生中和反应所放出的热量叫做中和热 | |
| C. | 氢氧化钡晶体与氯化铵晶体混合是吸热反应 | |
| D. | 化学反应中的能量变化与参加反应的物质的量成正比 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,B为18电子分子,其结构式为
,B为18电子分子,其结构式为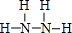 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
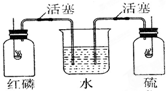 如图所示,红磷和硫磺在两纯氧集气瓶中燃烧,当火焰熄灭时,观察到的现象是( )
如图所示,红磷和硫磺在两纯氧集气瓶中燃烧,当火焰熄灭时,观察到的现象是( )| A. | 水迅速进入甲瓶和乙瓶 | B. | 水不进入甲瓶和乙瓶 | ||
| C. | 水只能进入甲瓶而不能进入乙瓶 | D. | 水只能进入乙瓶而不能进入甲瓶 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com