
| 实验序号 | 电极材料 | 水果品种 | 电极间距/cm | 电压/mV | |
| 1 | 锌 | 铜 | 菠萝 | 3 | 900 |
| 2 | 锌 | 铝 | 菠萝 | 3 | 650 |
| 3 | 锌 | 铝 | 苹果 | 3 | 450 |
| A. | 实验l 中锌为负极,电子由锌经导线流向铜 | |
| B. | 实验2 中铝为负极,铝失去电子,电流由锌经导线流向铝 | |
| C. | 实验3 中铝为负极,电极反应为Al-3e-═A13+ | |
| D. | 水果电池的电压只跟水果的品种有关 |
分析 A、实验l 锌、铜和水果形成原电池时,锌易失电子作负极,铜作正极,电子由负极经导线流向正极;
B、实验2锌、铝和水果形成原电池时,铝易失电子作负极,锌作正极,电流由正极经导线流向负极;
C、实验3锌、铝和水果形成原电池时,铝易失电子作负极,锌作正极;
D、根据图表中金属、电极和电压的关系分析.
解答 解:A、实验l 锌、铜和水果形成原电池时,锌易失电子作负极,铜作正极,所以电子由负极锌经导线流向正极铜,故A正确;
B、实验2锌、铝和水果形成原电池时,铝易失电子作负极,锌作正极,所以电流由正极锌经导线流向负极铝,故B正确;
C、实验3锌、铝和水果形成原电池时,铝易失电子作负极,电极反应为Al-3e-═A13+,故C正确;
D、根据图表知,当1、2比较时,电极材料不同,水果相同,导致电压不同,所以电压与电极材料有关;比较2、3时,电极材料相同,水果不同,导致电压不同,所以电压与水果有关,所以水果电池的电压跟水果的品种和电极材料都有关,故D错误;
故选D.
点评 本题考查了原电池原理,知道原电池中正负极的判断方法、会根据图表分析即可解答,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 氧原子采取的是sp2杂化 | B. | 分子中有3个σ键 | ||
| C. | 过氧化氢是极性分子 | D. | 每个氧原子上有两个孤对电子对 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
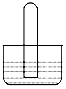
| A. | 若水槽中是NaOH溶液,试管中是CO2,可看到试管中液面上升很少 | |
| B. | 若水槽中是水,试管中是NO2,可看到液面上升并充满整个试管 | |
| C. | 若水槽中是水并滴有几滴酚酞,试管中是NH3,可看到试管中液体上升并呈红色 | |
| D. | 若水槽中是水并滴有几滴紫色石蕊,试管中是SO2,可看到液面上升并褪为无色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 图1现象说明该反应为放热反应 | |
| B. | 图2中b点的操作是压缩注射器体积 | |
| C. | c点:v (正)<v (逆) | |
| D. | 若不忽略体系温度变化,且没有能量损失,则T(d)>T(c) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只有②④ | B. | 只有①③ | C. | 只有②③ | D. | 只有①④ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 方案 | 现象或产物 |
| ①将铁片置于CuSO4溶液中 | 铁片上有亮红色物质析出 |
| ②将铁丝和铜丝分别在氯气中点燃 | 产物分别为FeC13和CuC12 |
| ③将铁片和铜片分别放入热浓硫酸中 | 产物分别为Fe2(SO4)3和CuSO4 |
| ④将铜片置于FeC13溶液中 | 铜片逐渐溶解 |
| ⑤将铁片和铜片插入盛有稀硫酸的烧杯中,并用导线连接 | 铁片溶解,铜片上有气泡产生 |
| A. | 2 种 | B. | 3 种 | C. | 4种 | D. | 5 种 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com