
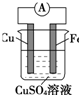
 如图所示,
如图所示,分析 该装置能自发的进行氧化还原反应而构成原电池,是将化学能转变为电能的装置,铁易失电子而作负极,负极上失电子发生氧化反应,正极铜电极上发生铜离子得电子的还原反应,据此分析.
解答 解:(1)该装置能自发的进行氧化还原反应而构成原电池,是将化学能转变为电能的装置,故答案为:原电池;化学;电;
(2)该装置能自发的进行氧化还原反应而构成原电池,铁易失电子而作负极,负极上失电子发生氧化反应,电极反应式为:Fe-2e-=Fe2+,故答案为:铁;Fe-2e-=Fe2+;
(3)正极铜电极上发生铜离子得电子的还原反应,电极反应式为:Cu2++2e-=Cu,总反应为:Fe+Cu2+=Cu+Fe2+,
故答案为:铜; Cu2++2e-=Cu; Fe+Cu2+=Cu+Fe2+.
点评 本题考查了原电池原理,明确正负极上得失电子及反应类型是解本题关键,比较简单.


科目:高中化学 来源: 题型:选择题
| 实验序号 | (1) | (2) | (3) |
| 取用盐酸的体积/mL | 25 | 25 | 25 |
| 取用混合物的质量/g | 1.32 | 1.54 | 2.20 |
| 生成气体的体积(标准状况)/mL | 336 | 392 | 448 |
| A. | 1.2 | B. | 1.4 | C. | 1.6 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
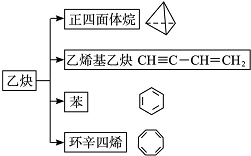
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3个B-F的键能相同 | B. | 3个B-F的键长相同 | ||
| C. | 3个B-F的键角均为120° | D. | 3个B-F的键均为σ键 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 溴水中有平衡:Br2+H2O?HBr+HBrO 加入AgNO3溶液后,溶液颜色变浅 | |
| B. | 合成 NH3反应,为提高 NH3的产率,理论上应采取相对较低温度的措施 | |
| C. | 高压比常压有利于合成SO3的反应 | |
| D. | 对CO(g)+NO2(g)?CO2(g)+NO(g) 平衡体系增大压强可使颜色变深 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | a-b=n+m | B. | b-a=n+m | ||
| C. | 原子序数:Y>X | D. | 离子半径:Ym-<Xn+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
| 实验步骤 | 实验现象 |
| ①将镁条用砂纸打磨后,放入试管中,加入少量水后,加热至水沸腾;再向溶液中滴加酚酞溶液 | A.浮在水面上,熔成小球,四处游动,发出“嘶嘶”声,随之消失,溶液变成红色. |
| ②在盛有冷水的烧杯中滴入几滴酚酞溶液,再将一小块金属钠放入其中 | B.有气体产生,溶液变成浅红色 |
| ③将镁条投入稀盐酸中 | C.剧烈反应,迅速产生大量无色气体 |
| ④将铝条投入稀盐酸中 | D.反应不十分剧烈;产生无色气体. |
| ⑤向A1Cl3溶液中滴加NaOH溶液至过量 | E.生成白色胶状沉淀,继而沉淀消失 |
| 实验内容 | ① | ② | ③ | ④ | ⑤ |
| 实验现象(填A~F) | B |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 标准状况下,11.2 L的丙烷所含的氢原子数为4NA | |
| B. | 16g甲烷所含电子数目为16NA | |
| C. | 标准状况下,11.2 L三氯甲烷所含分子数为0.5NA | |
| D. | 14 g乙烯的原子数为3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com