
下列有关金属及其化合物的说法中正确的是
A.铝和氢氧化钠溶液反应生成Al(OH)3和H2O
B.钠在空气中燃烧生成淡黄色的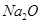
C.铁在高温下与水蒸气反应生成Fe2O3和H2
D.用碳酸钠和氢氧化钙反应制NaOH
科目:高中化学 来源: 题型:
碳元素是形成单质及其化合物种类最多的元素。回答下列有关问题。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图
a b
c
观察上述结构,判断a中碳原子的杂化方式为 ,b对应的物质是 ,
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为 。
(2)在C60单质中,微粒之间的作用力为 ,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1∶3,则K3C60属于 晶体。
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为 ;写出另一与CO互为等电子体的化学式 。
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4 的结构为 ;写出基态Ni原子的电子排布式 。
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。
(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能 ;CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大,其主要原因是 。
查看答案和解析>>
科目:高中化学 来源:2010-2011学年江苏省海门市高二下学期期末教学质量调研化学试题 题型:填空题
碳元素是形成单质及其化合物种类最多的元素。回答下列有关问题。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图
a  b
b 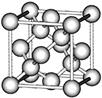 c
c 
观察上述结构,判断a中碳原子的杂化方式为 ,b对应的物质是 ,
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为 。
(2)在C60单质中,微粒之间的作用力为 ,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1∶3,则K3C60属于 晶体。
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为 ;写出另一与CO互为等电子体的化学式 。
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4的结构为 ;写出基态Ni原子的电子排布式 。
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特 点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。
点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。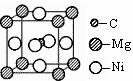
(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能 ;CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大,其主要原因是 。
查看答案和解析>>
科目:高中化学 来源:2012-2013学年广东省惠州市高三第三次调研考试理综化学试卷(解析版) 题型:选择题
下列有关硅及其化合物的说法正确的是
A.单质硅常用作半导体和光导纤维材料
B.硅在自然界中只以化合态的形式存在
C.SiO2与纯碱高温生成CO2,说明硅酸的酸性比碳酸强
D.SiO2是非金属氧化物,它不与任何酸反应
查看答案和解析>>
科目:高中化学 来源:2012届江苏省海门市高二下学期期末教学质量调研化学试题 题型:填空题
碳元素是形成单质及其化合物种类最多的元素。回答下列有关问题。
(1)碳元素可形成多种不同形式的单质,下列是几种单质的结构图
a  b
b 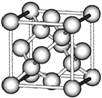 c
c 
观察上述结构,判断a中碳原子的杂化方式为 ,b对应的物质是 ,
c是C60的分子结构模型,在每个C60分子中形成的σ键数目为 。
(2)在C60单质中,微粒之间的作用力为 ,C60能与金属钾化合生成具有超导性的K3C60,在K3C60中阴阳离子个数比为1∶3,则K3C60属于 晶体。
(3)CO是碳元素的常见氧化物,分子中C原子上有一对孤对电子,与N2互为等电子体,则CO的结构式为 ;写出另一与CO互为等电子体的化学式 。
(4)CO可以和很多过渡金属形成配合物。金属镍粉在CO气流中轻微地加热,可生成液态的Ni(CO)4,用配位键表示Ni(CO)4 的结构为 ;写出基态Ni原子的电子排布式 。
(5)科学发现,C和Ni、Mg元素的原子形成的晶体也具有超导性,其晶胞的结构特点如右图,则该化合物的化学式为 ; C、Ni、Mg三种元素中,电负性最大的是 。

(6)碳的氢化物甲烷在自然界中广泛存在,其中可燃冰是有待人类开发的新能源。可燃冰是一种笼状结构,CH4分子存在于H2O分子形成的笼子中(如右图所示)。两种分子中,共价键的键能 ;CH4分子与H2O分子的分子量相差不大,但两种物质的熔沸点相差很大,其主要原因是 。

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com