
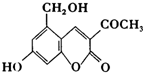
 “亮菌甲素”的结构简式为如图所示,它配以辅料丙二1,3,5醇溶成针剂用于临床,而假药“亮菌甲素”是用廉价的二甘醇作为辅料.二甘醇为工业溶剂,有很强的毒性,会使肾功能衰竭.请回答下列问题:
“亮菌甲素”的结构简式为如图所示,它配以辅料丙二1,3,5醇溶成针剂用于临床,而假药“亮菌甲素”是用廉价的二甘醇作为辅料.二甘醇为工业溶剂,有很强的毒性,会使肾功能衰竭.请回答下列问题:分析 (1)由结构简式可知分子式;
(2)丙二醇的分子式是C3H8O2,则2个-OH在不同的C原子上;
(3)含碳碳双键、酚-OH、醇-OH及-COOC-,结合烯烃、酚、醇、酯的性质分析;
(4)有3个吸收峰,其峰面积之比为2:2:1,则含3种位置的H,C、O元素的质量分数相同,且H的质量分数为9.4%,则$\frac{0.5×(1-9.4%)}{12}$:$\frac{0.5×(1-9.4%)}{16}$:$\frac{9.4%}{1}$=4:3:10,1mol二甘醇与足量金属钠反应生成1mol H2,则含2个-OH,二甘醇为HOCH2CH2OCH2CH2OH,与乙酸可发生酯化反应.
解答 解:(1)由结构简式可知分子式为C12H10O5,故答案为:C12H10O5;
(2)丙二醇的分子式是C3H8O2,则2个-OH在不同的C原子上,属于醇类的同分异构体的结构简式CH3CH(OH)CH2OH、CH2(OH)CH2 CH2(OH),
故答案为:CH3CH(OH)CH2OH、CH2(OH)CH2 CH2(OH);
(3)A.“亮菌甲素”含苯环和双键,能与H2发生加成反应,故A正确;
B.含双键,能使酸性KMnO4溶液褪色,故B错误;
C.“亮菌甲素”分子中含氧官能团为酚-OH、醇-OH及-COOC-,有3种,故C错误;
D.酚-OH、-COOC-及水解生成的酚-OH均与NaOH反应,1mol“亮菌甲素”最多与3mol NaOH反应,故D正确;
故答案为:AD;
(4)有3个吸收峰,其峰面积之比为2:2:1,则含3种位置的H,C、O元素的质量分数相同,且H的质量分数为9.4%,则$\frac{0.5×(1-9.4%)}{12}$:$\frac{0.5×(1-9.4%)}{16}$:$\frac{9.4%}{1}$=4:3:10,1mol二甘醇与足量金属钠反应生成1mol H2,则含2个-OH,二甘醇为HOCH2CH2OCH2CH2OH,与乙酸发生酯化反应为HOCH2CH2OCH2CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$HOCH2CH2OCH2CH2OOCCH3+H2O,
故答案为:HOCH2CH2OCH2CH2OH+CH3COOH$?_{△}^{浓H_{2}SO_{4}}$HOCH2CH2OCH2CH2OOCCH3+H2O.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,注意(4)中有机物的推断为解答的难点,题目难度中等.


 一本好题口算题卡系列答案
一本好题口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | ①②③⑥ | B. | ③④⑤⑥ | C. | ①②③④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | 26g乙炔所含共用电子对数目为3 NA | |
| B. | 标准状况下,11.2L的新戊烷所含的分子数为0.5 NA | |
| C. | 现有乙烯、丙烯、丁烯的混合气体共14g,其原子数为3 NA | |
| D. | 标准状况下,11.2 L CCl4所含分子数为0.5 NA |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 编号 | 电极材料 | 电解质溶液 | 灵敏电流计指针偏转方向 |
| 1 | Mg Al | 稀盐酸 | 偏向Al |
| 2 | Al Cu | 稀盐酸 | 偏向Cu |
| 3 | Al 石墨 | 稀盐酸 | 偏向石墨 |
| 4 | Mg Al | NaOH溶液 | 偏向Mg |
| 5 | Al Zn | 浓硝酸 | 偏向Al |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 只含一个双键的链状化合物 | B. | 含一个双键的环状化合物 | ||
| C. | 含一个三键的链状化合物 | D. | 含两个双键的链状化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 质子数为118,电子数为179,中子数为179 | |
| B. | 原子序数为179,质量数为297 | |
| C. | 与612C的相对原子质量之比为118:6 | |
| D. | 118297X经过一次α衰变得到的116号元素原子可表示116293X |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
| 编号 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径/10-10m | 0.77 | 0.99 | 1.86 | 0.75 | 1.17 | 1.02 | 1.43 | 0.71 | 1.52 | 0.89 |
| 最高正化合价 | +4 | +7 | +1 | +5 | +4 | +6 | +3 | +1 | +2 | |
| 最低负化合价 | -4 | -1 | -3 | -4 | -2 | -1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com