
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案科目:高中化学 来源:不详 题型:填空题
| 粒子符号 | 质子数Z | 中子数N | 核外电子数 | 质量数A |
| Cl | 17 | 20 | | |
| S2- | | | 18 | 32 |
| Al3+ | | 14 | | 27 |
| AYm- | | y | | A |
| AXn+ | x | | | A |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 电离能(kJ/mol) | I1 | I2 | I3 | I4 |
| A | 899.5 | 1757.1 | 14848.7 | 21006.6 |
| B | 738 | 1451 | 7733 | 10540 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.高聚氮晶体属于分子晶体 | B.高聚氮转化为N2是化学变化 |
| C.高聚氮是N2的一种同素异形体 | D.做炸药或高能材料可能是高聚氮潜在的应用 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
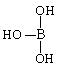 ,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式: (共4分)
,但硼酸溶于水后,1个硼酸分子与水作用,只能产生1个H+,请写出硼酸溶于水后溶液显酸性的离子方程式: (共4分)查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com