
【题目】根据问题填空:
(1)制造光导纤维的主要原料是(写化学式)
(2)硅是用于制造集成电路、电脑芯片、大阳能电池板(光电池,的半导体材料,硅原子结构示意图 .
(3)实验室不用带玻璃塞的试剂瓶盛放NaOH溶液的原因是:(用化学方程式表示) .
(4)硅酸凝胶经干燥脱水形成硅酸干胶,称为“硅胶”.它具有优良的性,常用于干燥剂,也可作催化剂的载体.
(5)硅酸钠(Na2SiO3)的水溶液俗称 , 常用作黏合剂和木材防火材料.
【答案】
(1)SiO2
(2)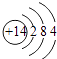
(3)SiO2+2NaOH=Na2SiO3+H2O
(4)吸附
(5)水玻璃(或泡花碱)
【解析】解:(1)二氧化硅具有良好的光学特性,是制备光导纤维主要原料,二氧化硅的化学式为:SiO2;所以答案是:SiO2;(2)硅原子是14号元素,质子数是14,三个电子层,每层电子数分别为2、8、4,所以硅原子结构示意图为 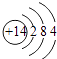 ,所以答案是:
,所以答案是: 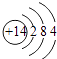 ;(3)玻璃中的二氧化硅与氢氧化钠反应生成具有粘性的硅酸钠溶液,能够将玻璃塞与玻璃瓶粘到一起,反应的方程式:SiO2+2NaOH=Na2SiO3+H2O,所以不能用带玻璃塞的试剂瓶盛放NaOH溶液,
;(3)玻璃中的二氧化硅与氢氧化钠反应生成具有粘性的硅酸钠溶液,能够将玻璃塞与玻璃瓶粘到一起,反应的方程式:SiO2+2NaOH=Na2SiO3+H2O,所以不能用带玻璃塞的试剂瓶盛放NaOH溶液,
所以答案是:SiO2+2NaOH=Na2SiO3+H2O;(4)硅酸凝胶经干燥脱水形成硅酸干胶,称为“硅胶”,硅胶表面积较大,有微孔,它具有优良的吸附性,吸水效果较好,且无毒,所以硅酸凝胶干燥后可作实验室、袋装食品和瓶装药品的干燥剂,硅胶疏松多孔,作干凝胶,可用作催化剂的载体,
所以答案是:吸附;(5)硅酸钠(Na2SiO3)的水溶液俗称“水玻璃”,是建筑行业经常使用的一种黏胶剂,也称为泡花碱,可用作肥皂填料,硅酸钠也可作木材和纺织品的防火剂,
所以答案是:水玻璃(或泡花碱).


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】随着科学技术的发展和环保要求的不断提高,CO2的捕集利用技术成为研究的重点.
完成下列填空:
(1)目前国际空间站处理CO2的一个重要方法是将CO2还原,所涉及的反应方程式为:
CO2(g)+4H2(g)CH4(g)+2H2O(g)
已知H2的体积分数随温度的升高而增加.
若温度从300℃升至400℃,重新达到平衡,判断下列表格中各物理量的变化.(选填“增大”、“减小”或“不变”)
v正 | v逆 | 平衡常数K | 转化率α |
(2)相同温度时,上述反应在不同起始浓度下分别达到平衡,各物质的平衡浓度如下表:
[CO2]/molL﹣1 | [H2]/molL﹣1 | [CH4]/molL﹣1 | [H2O]/molL﹣1 | |
平衡Ⅰ | a | b | c | d |
平衡Ⅱ | m | n | x | y |
a、b、c、d与m、n、x、y之间的关系式为 .
(3)碳酸:H2CO3 , Ki1=4.3×10﹣7 , Ki2=5.6×10﹣11
草酸:H2C2O4 , Ki1=5.9×10﹣2 , Ki2=6.4×10﹣5
0.1mol/LNa2CO3溶液的pH0.1mol/LNa2C2O4溶液的pH.(选填“大于”“小于”或“等于”)
等浓度的草酸溶液和碳酸溶液中,氢离子浓度较大的是 . 若将等浓度的草酸溶液和碳酸溶液等体积混合,溶液中各种离子浓度大小的顺序正确的是 . (选填编号)
a.[H+]>[HC2O4﹣]>[HCO3﹣]>[CO32﹣] b.[HCO3﹣]>[HC2O4﹣]>[C2O42﹣]>[CO32﹣]
c.[H+]>[HC2O4﹣]>[C2O42﹣]>[CO32﹣] d.[H2CO3]>[HCO3﹣]>[HC2O4﹣]>[CO32﹣]
(4)人体血液中的碳酸和碳酸氢盐存在平衡:H++HCO3﹣H2CO3 , 当有少量酸性或碱性物质进入血液中时,血液的pH变化不大,用平衡移动原理解释上述现象.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图表示AlCl3溶液与NaoH溶液相互滴加过程中微粒的量的关系曲线,下列判断错误的是( ) 
A.①线表示Al3+的物质的量的变化
B.x表示AlCl3的物质的量
C.③线表示Al(OH)3的物质的量的变化
D.④线表示 ![]() 的物质的量的变化
的物质的量的变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列俗名与化学式对应的是( )
A. 石膏:CaSO4·2H2OB. 碳铵:(NH4)2CO3
C. 重晶石:BaCO3D. 芒硝:Na2SO4·12H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】联氨(又称肼,N2H4 , 无色液体)是一种应用广泛的化工原料,可用作火箭燃料.回答下列问题:
(1)联氨分子的电子式为 , 其中氮的化合价为 .
(2)实验室中可用次氯酸钠溶液与氨反应制备联氨,反应的化学方程式为 .
(3)①2O2(g)+N2(g)═N2O4(l)△H1
②N2(g)+2H2(g)═N2H4(l)△H2
③O2(g)+2H2(g)═2H2O(g)△H3
④2N2H4(l)+N2O4(l)═3N2(g)+4H2O(g)△H4=﹣1048.9kJmol﹣1
上述反应热效应之间的关系式为△H4= , 联氨和N2O4可作为火箭推进剂的主要原因为 .
(4)联氨为二元弱碱,在水中的电离方式与氨相似.联氨第一步电离反应的平衡常数值为(已知:N2H4+H+N2H5+的K=8.7×107;Kw=1.0×10﹣14).联氨与硫酸形成的酸式盐的化学式为 .
(5)联氨是一种常用的还原剂.向装有少量AgBr的试管中加入联氨溶液,观察到的现象是 . 联氨可用于处理高压锅炉水中的氧,防止锅炉被腐蚀.理论上1kg的联氨可除去水中溶解的O2kg;与使用Na2SO3处理水中溶解的O2相比,联氨的优点是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红磷(P)和白磷(P4)均为磷的同素异形体.已知:
P4(白磷、s)+5O2(g)═P4O10(s)△H═﹣2983.2kJ/mol
P(红磷、s)+ ![]() O2(g)═
O2(g)═ ![]() P4O10(s)△H═﹣738.5kJ/mol
P4O10(s)△H═﹣738.5kJ/mol
写出白磷转化为红磷的热化学方程式 , 由此可知,红磷比白磷 . (填“稳定”或“不稳定”)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,现有0.1mol/L的NH4HCO3溶液,pH=7.8.已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如图所示.下列说法正确的是( ) 
A.当溶液的pH=9时,溶液中存在下列关系:c(NH4+)>c(HCO3﹣)>c(NH3H2O)>c(CO32﹣)
B.NH4HCO3溶液中存在下列守恒关系:c(NH4+)+c(NH3H2O)+c(H+)=c(OH﹣)+2c(CO32﹣)+c(H2CO3)
C.往该溶液中逐滴滴加氢氧化钠时NH4+和HCO3﹣浓度逐渐减小
D.通过分析可知常温下Kb(NH3H2O)>Ka1(H2CO3)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2 , 恰好使溶液中的SO42﹣离子完全沉淀;如加入足量强碱并加热可得到c mol NH3 , 则原溶液中的Al3+浓度(mol/L)为( )
A.![]()
B.![]()
C.![]()
D.![]()
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com