
| A. | N2既是氧化产物又是还原产物 | |
| B. | 反应通式配平为6NOx+4xNH3=(3+2x)N2+6xH2O | |
| C. | 当x=1时,每生成2.5mol N2,被氧化的气体有3mol | |
| D. | 当x=2时,有1mol气体被还原时,转移的电子为4mol |
分析 NOx+NH3→N2+H2O,只有N元素的化合价变化,则N2既是氧化产物又是还原产物,x=1时,N元素的化合价变化为+2→0,-3→0,则反应为6NO+4NH3=5N2+6H2O,生成5molN2被氧化的气体为4mol氨气;当x=2时,N元素的化合价变化为+4→0,-3→0,则反应为6NO2+8NH3═7N2+12H2O,6mol二氧化氮被还原,转移24mol电子,以此来解答.
解答 解:A.只有N元素的化合价变化,则N2既是氧化产物又是还原产物,故A正确;
B.由原子守恒可知,反应通式配平表示为:6NOx+4xNH3═(3+2x)N2+6xH2O,故B正确;
C.当x=1时,N元素的化合价变化为+2→0,-3→0,则反应为6NO+4NH3═5N2+6H2O,生成5molN2被氧化的气体为4mol氨气,则每生成2.5 mol N2,被氧化的气体有2mol,故C错误;
D.当x=2时,N元素的化合价变化为+4→0,-3→0,则反应为6NO2+8NH3═7N2+12H2O,6mol二氧化氮被还原,转移24mol电子,则1 mol气体被还原,转移电子4 mol,故D正确;
故选C.
点评 本题考查氧化还原反应,为高频考点,把握反应中元素的化合价变化为解答的关键,侧重分析与应用能力及转移电子分析的考查,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | KI溶液在空气久置变黄:4I-+O2+4H+=2I2+2H2O | |
| B. | 用稀盐酸除去久存石灰水的烧杯内壁上的固体:2H++Ca(OH)2=Ca2++2H2O | |
| C. | 用酸性KMnO4溶液除去CO2中SO2:3SO2+2MnO4-+4H+=3SO42-+2MnO2↓+H2O | |
| D. | 用足量饱和Na2CO3溶液吸收制备的乙酸乙酯:CO32-+CH3COOH=HCO3-+CH3COO- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 体积不变,增加H2O(g)的量 | |
| B. | 保持体积不变,充入Ne使体系压强增大 | |
| C. | 将容器的体积缩小一半 | |
| D. | 压强不变,充入He使容器的体积增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②④⑤ | B. | ③④⑤ | C. | ③④⑥ | D. | ①②③④⑤⑥ |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
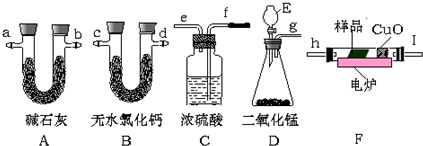
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,11.2L四氯化碳所含分子数为0.5 NA | |
| B. | 1mol/L的盐酸溶液中,所含氯化氢分子数为NA | |
| C. | 80g硝酸铵含有氮原予数为2NA | |
| D. | 1mol氯气和铁反应时转移的电子数为3NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电解饱和食盐水时,阳极的电极反应式为:2Cl--2e-=Cl2↑ | |
| B. | 氢氧燃料电池的负极反应式:O2+2H2O+4e-=4OH- | |
| C. | 在铁的表面镀上一层锌,铁作阳极,电极反应式为:Zn2++2e-=Zn | |
| D. | 钢铁发生电化学腐蚀的正极反应式:Fe-2e-=Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
 ,最简单烯烃的结构简式为
,最简单烯烃的结构简式为 ,最简单芳香烃的分子式为C6H6,C4H10 的一氯代物有4种,C5H12 的同分异构体中沸点最低的物质 的结构简式为
,最简单芳香烃的分子式为C6H6,C4H10 的一氯代物有4种,C5H12 的同分异构体中沸点最低的物质 的结构简式为 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com