
【题目】氨是最重要的氮肥,是产量最大的化工产品之一。德国人哈伯在1905年发明了合成氨的方法,其合成原理为:N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ/mol,他因此获得了1918年诺贝尔化学奖。密闭容器中,使2 mol N2和6 mol H2混合发生反应:N2(g)+3H2(g)
2NH3(g) ΔH=-92.4 kJ/mol,他因此获得了1918年诺贝尔化学奖。密闭容器中,使2 mol N2和6 mol H2混合发生反应:N2(g)+3H2(g)![]() 2NH3(g)(正反应为放热反应)。
2NH3(g)(正反应为放热反应)。
(1)当反应达到平衡时,N2和H2的浓度比是___________;N2和H2的转化率比是_____________。
(2)升高平衡体系的温度(保持体积不变),混合气体的平均相对分子质量____________,密度_____________。(填“变大”、“变小”或“不变”)
(3)当达到平衡时,充入氩气,并保持压强不变,平衡将_____________(填“正向”、“逆向”或“不”)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将________(填“向左移动”、“向右移动”或“不移动”)。达到新平衡后,容器内温度________(填“大于”、“小于”或“等于”)原来的2倍。
【答案】 1∶3 1∶1 变小 不变 逆向 向左移动 小于
【解析】试题分析:在密闭容器中,使2 mol N2和6 mol H2混合发生下列反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=-92.4 kJ·mol-1,正反应为放热反应。
2NH3(g) ΔH=-92.4 kJ·mol-1,正反应为放热反应。
(1)因为原始投料时N2和H2的物质的量之比为1:3,在反应过程中,两者的变化量之比也是1:3,所以当反应达到平衡时,N2和H2的物质的量之比必然还是1:3,所以其浓度比是1:3;转化率等于变化量占起始量的百分数,原始投料时N2和H2的物质的量之比为1:3,两者的变化量之比也是1:3,所以N2和H2的转化率之比是1:1。
(2)升高平衡体系的温度(保持体积不变),化学平衡将向吸热反应方向移动,即向逆反应方向移动,混合气体的总物质的量增大,而质量守恒,所以混合气体的平均相对分子质量变小。因为质量守恒、体积不变,所以密度不变。
(3)当达到平衡时,充入氩气,并保持压强不变,则容器的体积必须增大,反应混合物中各组分的浓度都要减小,这相当于减压,化学平衡将气体体积增大的方向移动,即逆向)移动。
(4)若容器恒容、绝热,加热使容器内温度迅速升至原来的2倍,平衡将向吸热反应方向移动,即向左移动。达到新平衡后,容器内温度小于原来的2倍。


科目:高中化学 来源: 题型:
【题目】(9分)认真观察下列装置,回答下列问题:
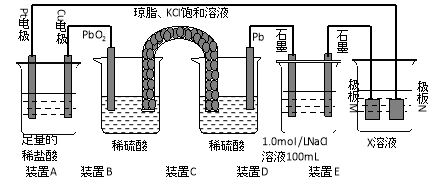
⑴装置B中PbO2上发生的电极反应方程式为 。
⑵装置A中总反应的离子方程式为 。
⑶若装置E中的目的是在Cu材料上镀银,则X为 ,极板N的材料为 。
若装置E的目的是验证金属的电化学防腐,则极板N的材料为__________________ 。
⑷当装置A中Cu电极质量改变6.4g时,装置D中产生的气体体积为 L(标准状况下)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新冠病毒由蛋白质外壳和单链核酸组成,直径大约在60~140nm,怕酒精,不耐高温。下列说法正确的是
A.病毒由碳、氢、氧三种元素组成
B.新冠病毒扩散到空气中不可能形成胶体
C.医用酒精能用于消毒是因为它有强氧化性
D.高温可使蛋白质发生变性
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有A、B、C三种化合物,各取40g相混合,完全反应后,得18gB、49gC、还有D生成.现将20gA和11gB反应,能生成0.25mol D,则D的相对分子质量为( )
A. 424 B. 212 C. 116.6 D. 106
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,C(s)和H2O(g)在密闭容器中发生下列反应:
①C(s)+H2O(g) ![]() CO(g)+H2(g) ②CO(g)+H2O(g)
CO(g)+H2(g) ②CO(g)+H2O(g) ![]() CO2(g)+H2(g)
CO2(g)+H2(g)
当反应达到平衡时,测得c(H2)=1.9 mol·L-1,c(CO)=0.1 mol·L-1,则CO2的浓度为
A. 0.1 mol·L-1 B. 0.9 mol·L-1 C. 1.8 mol·L-1 D. 1.9 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化硅是一种高温陶瓷材料,它的硬度大、熔点高、化学性质稳定,工业上曾普遍采用高纯硅与纯氮气在1 300 ℃时反应获得。
(1)根据 性质,推测氮化硅陶瓷的用途是(填字母)。
a.制汽轮机叶片 b.制有色玻璃
c.制永久性模具 d.制造柴油机
(2)画出N的原子结构示意图 , 已知得电子能力N>Si,请写出氮化硅的化学式:。
(3)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应。试推测该陶瓷被氢氟酸腐蚀的化学方程式:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图中的每一方格表示相关的一种反应物或生成物。其中B是一种单质,其余物质也都是有B元素的化合物。C是一种钠盐,E是C对应的酸,B的结构类似金刚石,D为B的氧化物(其他不含B元素的反应产物以及各步反应添加的必要试剂和反应条件已被略去),请填写空白:
(1)A、D、E的化学式分别为、、。
(2)A和B的互相转化在工业上有什么实际意义?
。
(3)写出D→C反应的化学方程式:
。
(4)写出E→D反应的化学方程式:。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学与生活密切相关。下列说法不正确的是
A.矿泉水富含人体必需的营养物质
B.用75%的酒精灭活新型冠状病毒
C.食物纤维不能被人体吸收利用,却是不可或缺的一部分
D.过多服用阿司匹林(乙酰水杨酸)引起酸中毒,可注射NaHCO3溶液解毒
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.电解MgCl2饱和溶液可制得金属镁
B.用浓硫酸与铁反应能增大生成H2的速率
C.电解饱和食盐水,水的电离平衡正向移动
D.纯银器在空气中露置其表面因电化学腐蚀渐渐变暗
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com