
| A. | 放电时锌做负极 | |
| B. | 充电时电池的正极和电源的正极相连 | |
| C. | 充电时氢氧化铁被氧化 | |
| D. | 放电时每转移3 mol e-,有2 mol FeO42-被还原 |
分析 由反应可知,放电时Zn为负极,电极方程式为Zn-2e-+2OH-=Zn(OH)2,K2FeO4在正极上发生还原反应,电极方程式为FeO42-+4H2O+3e-═Fe(OH)3+5OH-;充电时电池的正极与电源的正极相连为阳极,阳极发生氧化反应,充电时的反应为放电的逆反应,以此来解答.
解答 解:A.放电时,Zn失去电子,发生Zn-2e-+2OH-=Zn(OH)2,则放电时锌做负极,故A正确;
B.充电时电池的正极和电源的正极相连,作阳极,故B正确;
C.充电时Fe(OH)3失电子生成有KOH生成K2FeO4,Fe的化合价升高被氧化,故C正确;
D.放电时,Fe化合价由+6价降低为+3价,则放电时每转移3mol电子,正极有1molK2FeO4被还原,故D错误;
故选D.
点评 本题考查化学电源新型电池,明确信息中的总反应及放电为原电池反应、充电为电解池反应是解答本题的关键,注意发生的电极反应,题目难度中等.


 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案科目:高中化学 来源: 题型:选择题
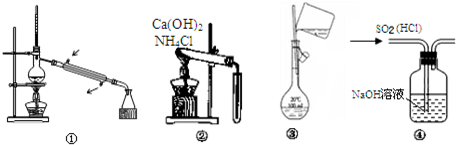
| A. | 图①常用于分离沸点不同且彼此互溶的液态混合物 | |
| B. | 图②可用于实验室制备并收集少量的NH3 | |
| C. | 图③表示的是实验室配制溶液转移过程 | |
| D. | 图④可用于除去SO2中的HCl气体 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 5?mol•L-1 | B. | 2.5?mol•L-1 | C. | ?d/400 mol•L-1 | D. | ?d/200mol•L-1 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 玻璃、陶瓷、水泥 | B. | 塑料,合成纤维、橡胶 | ||
| C. | 青铜、碳素钢、硬铝 | D. | 玻璃钢、聚乙烯、超导陶瓷 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K+、SO42-、CO32- | B. | Al3+、Na+、NO3- | C. | NH4+、OH-、SO32- | D. | Ag+、Cu2+、HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
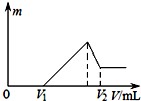
| A. | 向硫酸溶液中加入氢氧化钡溶液 | |
| B. | 向碳酸氢钠溶液中加入氯化钙 | |
| C. | 向硫酸、硫酸镁、硫酸铝的混合溶液中逐滴加入氢氧化钠溶液直至过量 | |
| D. | 向氯化铝溶液中加入过量氢氧化钠溶液 |
查看答案和解析>>
科目:高中化学 来源:2016-2017学年江西省高二上第一次月考化学卷(解析版) 题型:选择题
一定温度下,在密闭容器中发生如下反应:N2O4(g) 2NO2(g)△H>0,反应达到平衡时,下列说法不正确的是( )
2NO2(g)△H>0,反应达到平衡时,下列说法不正确的是( )
A.若缩小容器的体积,则容器中气体的颜色先变深后又变浅,且比原平衡颜色深
B.若压强不变,向容器中再加入一定量的N2O4,再次达到平衡时各种物质的百分含量不变
C.若体积不变,向容器中再加入一定量的N2O4,平衡向逆反应方向移动,再次平衡时N2O4的转化率将降低
D.若体积不变,升高温度,再次平衡时体系颜色加深
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com