
| A.H与D,16O与18O互为同位素;H216O、D216O、H218O、D218O互为同素异形体 |
| B.在SiO2晶体中,1个Si原子和2个O原子形成2个共价键 |
| C.HI的相对分子质量大于HF,所以HI的沸点高于HF |
| D.由ⅠA族和ⅥA族元素形成的原子个数比为1∶1、电子总数为38的化合物,是含有共价键的离子型化合物 |
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:不详 题型:填空题

查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
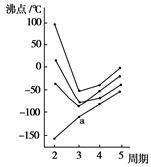
| A.H2S | B.HCl | C.PH3 | D.SiH4 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 键和1个大
键和1个大 键,C2H2是非极性分子
键,C2H2是非极性分子
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①②③④⑤⑥ | B.①②③④⑤ | C.①②③④ | D.①②③ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.附着在试管内壁上的AgCl固体可用氨水溶解而洗去 |
| B.可用氨水鉴别AlCl3、AgNO3和CuSO4三种溶液 |
| C.向氨水中滴加CuSO4溶液至过量,先产生蓝色沉淀,然后沉淀溶解并得到深蓝色溶液 |
| D.加热碘单质,产生紫色碘蒸气,这个过程只克服范德华作用力 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.P4和CH4都是正四面体分子且键角都为109o28ˊ |
| B.CO2、NH3、BF3分子中所有原子的最外层电子都满足了8e-稳定结构 |
| C.具有共价键的晶体叫做原子晶体,一定具有高的熔、沸点及硬度 |
| D.H—F的键能为568 kJ/mol,H—Cl的键能为431.8 kJ/mol,这可以说明HF分子比HCl分子稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 元素代号 | W | R | X | Y | Z | Q | M |
| 原子半径/nm | 0.037 | 0.186 | 0.074 | 0.075 | 0.077 | 0.110 | 0.160 |
| 主要化合价 | +1 | +1 | -2 | -3,+5 | +2,+4 | -3,+5 | +2 |

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com