
 按要求问答下列问题
按要求问答下列问题| 1 |
| 3 |
| 1 |
| 12 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |
| 1 |
| 2 |


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案科目:高中化学 来源: 题型:
| A、O2中既有σ键又有π键 |
| B、该反应中,每消耗11.2L的氧气,乙醚失去的电子数为12.4×10-23 |
| C、1-乙氧基氢过氧化物中只有极性键没有非极性键 |
| D、起麻醉作用的是l-乙氧基氢过氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、由分子组成的物质中一定存在共价键 |
| B、由非金属组成的化合物不一定是共价化合物 |
| C、只有共价化合物里存在共价键 |
| D、离子化合物里只存在离子键 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:
过渡金属元素氧化物的应用研究是目前科学研究的前沿之一,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
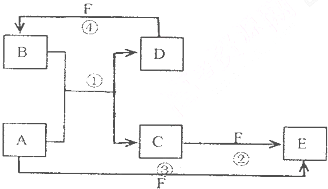
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③⑥⑨ | B、②④⑤⑨ |
| C、③④⑦⑧ | D、①⑧⑨ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com