
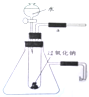
 用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来.
用脱脂棉包住0.2g过氧化钠粉末,置于石棉网上,往脱脂棉上滴几滴水,可观察到脱脂棉剧烈燃烧起来.分析 (1)脱脂棉剧烈燃烧起来说明反应放热,是过氧化钠和水反应生成氢氧化钠和氧气;
(2)①可用带火星的木条靠近a处,如果木条复燃,则有氧气生成,反之无氧气生成;
②氧气具有能使带火星的木条复燃的性质;
③气体具有热胀冷缩的性质,该反应放出的热量能使集气瓶内空气的压强增大,据此分析问题.
解答 解:( 1)脱脂棉剧烈燃烧说明具备燃烧的条件,试管内空气较少,若剧烈燃烧应该有大量氧气,只有该反应是放热反应才能使燃料温度达到着火点,根据题意知脱脂棉剧烈燃烧起来该反应有氧气生成且放热,过氧化钠和水反应生成氢氧化钠和氧气,反应的化学方程式为:2Na2O2+2H2O=4NaOH+O2↑,
故答案为:反应放热,2Na2O2+2H2O=4NaOH+O2↑;
(2)①氧气具有使带火星的木条复燃的性质,所以可用带火星的木条靠近a处,如果木条复燃,则有氧气生成,反之无氧气生成,操作是打开活塞(或阀门)向试管内包有过氧化钠的石棉网上滴几滴水,用带火星的木条靠近a处,
故答案为:打开活塞(或阀门)向试管内包有过氧化钠的石棉网上滴几滴水,用带火星的木条靠近a处;
②氧气具有使带火星的木条复燃的性质,用带火星的木条靠近a处,木条复燃,则证明有氧气生成,
故答案为:带火星的木条复燃;
③气体具有热胀冷缩的性质,如果该反应放热,放出的热量能使集气瓶内空气的压强增大;如果b导管插入盛水的小烧杯中,有气泡冒出,证明此反应放热,
故答案为:将导管b置于水槽中.再打开分液漏斗的开关,发现b处有气泡放出.
点评 本题考查了过氧化钠和水反应的实验,难度不大,解答时要从实验现象方面进行分析、判断,从而得出正确的结论.


科目:高中化学 来源: 题型:解答题
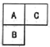 短周期元素A、B、C在元素周期表中的位置关系如图所示,B元素原子的核外电子数等于C元素原子序数的2倍.
短周期元素A、B、C在元素周期表中的位置关系如图所示,B元素原子的核外电子数等于C元素原子序数的2倍.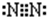 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
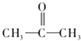
 .
. .
.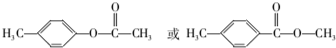 .
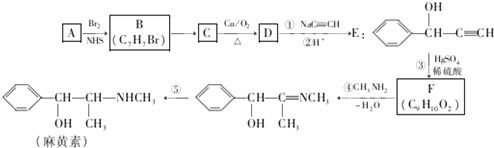
. 的合成路线,其它试剂及溶剂任选.
的合成路线,其它试剂及溶剂任选.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Fe(OH)3胶体 | B. | Fe(OH)3沉淀 | C. | FeCl3溶液 | D. | 油水混合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 沸点:CH4>NH3>H2O | B. | 得电子能力:C>N>O | ||
| C. | 酸性:H2SO4>HClO4>H3PO4 | D. | 碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在0.1 mol•L-1NaHCO3溶液中:c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) | |
| B. | 在0.1 mol•L-1Na2CO3溶液中:c(OH-)-c(H+)=c(HCO3-)+2c(H2CO3) | |
| C. | 向0.2 mol•L-1NaHCO3溶液中加入等体积0.1 mol•L-1NaOH溶液:c(CO32-)>c(HCO3-)>c(OH-)>c(H+) | |
| D. | 常温下,CH3COONa和CH3COOH混合溶液[pH=7,c(Na+)=0.1 mol•L-1]:c(Na+)>c(CH3COO-)>c(CH3COOH)>c(H+)=c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
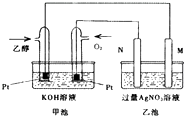 如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:
如图是一个乙醇燃料电池工作时的示意图,乙池中的两个电极一个是石墨电极,一个是铁电极,工作时M、N两个电极的质量都不减少,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质的氧化性逐渐减弱 | B. | 单质的熔、沸点逐渐降低 | ||
| C. | 单质的密度逐渐降低 | D. | 气态氢化物的稳定性逐渐增强 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com