
分析 (1)含碳碳双键、三键、酚-OH、-CHO的有机物能使溴的四氯化碳溶液褪色;
(2)庚烷中含7个C,16个H;
(3)水中氢键多;
(4)苯为非极性分子,水为极性分子;
(5)某烃的分子量为40,$\frac{40}{12}$=3…4;
(6)乙苯能被高锰酸钾氧化,苯不能;
(7)丙烯能使溴水、高锰酸钾褪色,丙烷不能;
(8)相对分子质量为46,含2个C;
(9)含C质量分数为85.7%的烃为烯烃或环烷烃;
(10)苯为平面正六边形.
解答 解:(1)含碳碳双键、三键、酚-OH、-CHO的有机物能使溴的四氯化碳溶液褪色,则能够使溴的四氯化碳溶液褪色的物质如CH≡CH,故答案为:CH≡CH;
(2)庚烷中含7个C,16个H,分子式为C7H16,故答案为:C7H16;
(3)水中氢键多,则乙醇的沸点比水低,故答案为:低;
(4)苯为非极性分子,水为极性分子,则苯不溶于水,故答案为:不溶;
(5)某烃的分子量为40,$\frac{40}{12}$=3…4,则分子式为C3H4,故答案为:C3H4;
(6)乙苯能被高锰酸钾氧化,苯不能,则鉴别试剂为高锰酸钾,故答案为:高锰酸钾;
(7)丙烯能使溴水、高锰酸钾褪色,丙烷不能,则鉴别试剂为溴水或高锰酸钾,故答案为:溴水或高锰酸钾;
(8)相对分子质量为46,含2个C,C的质量分数为$\frac{12×2}{46}$×100%=52.2%,故答案为:52.2%;
(9)含C质量分数为85.7%的烃为烯烃或环烷烃,最简式为CH2,故答案为:CH2;
(10)苯为平面正六边形,则分子中6个C、6个H共面,共12个原子,故答案为:12.
点评 本题考查有机物的结构与性质,为高频考点,把握官能团与性质的关系为解答的关键,侧重分析与应用能力的考查,注意常见有机物的性质、组成及应用,题目难度不大.


科目:高中化学 来源: 题型:选择题
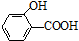 )存在分子内氢键,对羟基苯甲酸 (
)存在分子内氢键,对羟基苯甲酸 ( 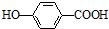 )存在分子间氢键.则两者的熔点、沸点的相对大小关系是( )
)存在分子间氢键.则两者的熔点、沸点的相对大小关系是( )| A. | 前者>后者 | B. | 前者<后者 | C. | 前者=后者 | D. | 无法估计 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
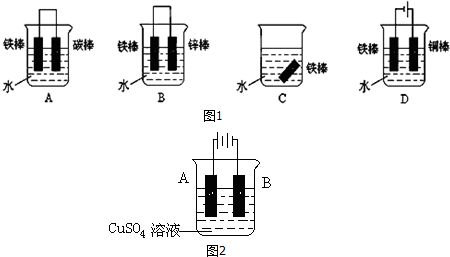
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:解答题
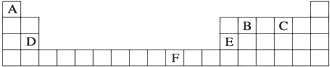
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铅笔芯的原料是金属铅,儿童在使用时不可用嘴吮咬铅笔,以免引起铅中毒 | |
| B. | 一氧化碳有毒,生有煤炉的居室,可放置数盆清水,这样可有效地吸收一氧化碳,防止煤气中毒 | |
| C. | 为解决能源短缺的问题,使用催化剂将水变成油 | |
| D. | 大气中化学污染物主要是氮氧化物和硫氧化物 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | K 37ClO3与浓盐酸(HCl)在加热下生成氯气的化学方程式:K 37ClO3+6HCl═K 37Cl+3Cl2↑+3H2O | |
| B. | 表示氢气燃烧热的热化学方程式:H2 (g)+$\frac{1}{2}$O2(g)=H2O(g);△H=-241.8 kJ/mol | |
| C. | 将1~2 mL氯化铁饱和溶液逐滴加到20 mL 沸水中所发生反应的离子方程式:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe (OH)3(胶体)+3H+ | |
| D. | 在氢氧化钡溶液中滴入硫酸氢钠溶液至中性:Ba2++OH-+H++SO42-=BaSO4↓+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 摩尔是七个基本物理量之一 | |
| B. | 阿伏加德罗常数就是6.02×1023mol-1 | |
| C. | 1mol氢的质量是2g | |
| D. | 1个甲烷分子的质量是2.66×10-23g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com