
| A. | 石墨和金刚石不能相互转化 | |
| B. | 金刚石比石墨稳定 | |
| C. | 破坏1mol金刚石中的共价键消耗的能量比石墨多 | |
| D. | 1 mol石墨比1 mol金刚石的总能量低 |
分析 在100kPa时,1mol石墨转化为金刚石,要吸收1.895kJ的能量说明石墨的能量低于金刚石的能量,能量低的物质稳定;化学变化的特征是生成新物质.
解答 解:1mol石墨转化为金刚石,要吸收1.895kJ的能量说明石墨的能量低于金刚石的能量
A、金刚石和石墨是同素异形体,同素异形体之间的转化属于化学变化,故A错误;
B、石墨的能量比金刚石低,能量越低越稳定,石墨比金刚石稳定,故B错误;
C、石墨的能量比金刚石低,破坏1mol金刚石中的共价键消耗的能量比石墨少,故C错误;
D、金刚石比石墨能量高,即1 mol石墨比1 mol金刚石的总能量高,故D正确;
故选:D.
点评 本题主要考查金刚石和石墨的转化以及涉及到的能量变化,难度不大,需要掌握的是能量低的物质稳定.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 在紫外线、饱和Na2SO4、CuSO4溶液、福尔马林等作用下,蛋白质均会发生变性 | |
| B. | 油脂属于高分子化合物,是混合物 | |
| C. | 在一定条件下,氨基酸之间能发生反应,合成更加复杂的化合物 | |
| D. | 检验淀粉在稀硫酸催化条件下水解产物的方法是:取适量水解液于试管中,加入少量新制Cu(OH)2悬浊液,加热,观察是否有砖红色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:多选题
| A. | CO2(CO):气体通过灼热的CuO | |
| B. | Cl2(SO2):通入盛有品红溶液的洗气瓶 | |
| C. | NO(NO2):通过水洗,再干燥后,用向下排空气法收集 | |
| D. | H2(CO2):依次通过盛有氢氧化钠溶液和浓硫酸的洗气瓶 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
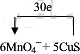
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 乙烯和环丙烷(C3H6)组成的28g混合气体中含有2 NA个碳原子 | |
| B. | 7.8 g苯中含有0.3NA个碳碳双键,0.3NA个碳碳单键 | |
| C. | 标准状况下,2.24L已烷含有分子的数目为0.1NA | |
| D. | 1molCH4O中含有C-H键的数目为4NA |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 编号 | H2O2溶液 | 酸性KMnO4溶液 | 温度/℃ | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | ||
| ① | 0.10 | 2.0 | 0.010 | 4.0 | 25 |
| ② | 0.20 | 2.0 | 0.010 | 4.0 | 25 |
| ③ | 0.20 | 2.0 | 0.010 | 4.0 | 50 |
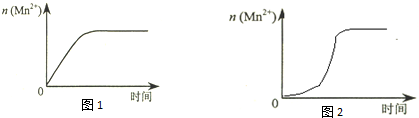
| 编号 | H2O2溶液 | 酸性KMnO4溶液 | 温度/℃ | 再向试管中加入少量固体 | ||
| 浓度/mol•L-1 | 体积/mL | 浓度/mol•L-1 | 体积/mL | |||
| ④ | 0.10 | 2.0 | 0.010 | 4.0 | 25 | |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
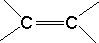 )中的π键不能自由旋转,因此CH3CH=CHCH3有两种顺反异构体.苏丹红Ⅰ号的分子结构如图1所示,分子中所有原子有(填“有”或“不”)可能在同一平面上.它的另一顺反异构体的结构简式为
)中的π键不能自由旋转,因此CH3CH=CHCH3有两种顺反异构体.苏丹红Ⅰ号的分子结构如图1所示,分子中所有原子有(填“有”或“不”)可能在同一平面上.它的另一顺反异构体的结构简式为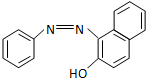 .苏丹红Ⅰ号在水中的溶解度很小,微溶于乙醇,若把羟基取代在对位形成图2所示结构,则其溶解度会增大,熔点升高(填“升高”或“降低”).下面两种物质的物理性质存在上述差异的原因可能是苏丹红I号形成分子内氢键,而修饰后的分子形成分子间氢键,分子间氢键有利于增加分子间作用力,从而有利于增大化合物的溶解度和提高熔点.
.苏丹红Ⅰ号在水中的溶解度很小,微溶于乙醇,若把羟基取代在对位形成图2所示结构,则其溶解度会增大,熔点升高(填“升高”或“降低”).下面两种物质的物理性质存在上述差异的原因可能是苏丹红I号形成分子内氢键,而修饰后的分子形成分子间氢键,分子间氢键有利于增加分子间作用力,从而有利于增大化合物的溶解度和提高熔点.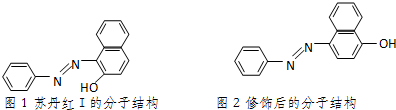
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com