

 互为同分异构体,则其物质结构简式为HCOOCH(CH3)CH2CH3
互为同分异构体,则其物质结构简式为HCOOCH(CH3)CH2CH3 +CH3CH2CH2OH→
+CH3CH2CH2OH→ +CH3OH
+CH3OH 的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
的合成路线流程图(无机试剂任选).合成路线流程图示例如下:
分析 丙酮和HCN发生加成反应生成A,A的结构简式为:(CH3)2C(OH)CN,A发生消去反应生成CH2=C(CH3)CN,CH2=C(CH3)CN和水反应生成CH2=C(CH3)COOH,CH2=C(CH3)COOH和甲醇反应生成MMA,MMA的结构简式为:CH2=C(CH3)COOCH3,在一定条件下,丙烯和一氧化碳、氢气反应生成B,B的结构简式为: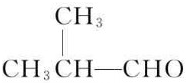 ,B能被新制氢氧化铜氧化、然后酸化生成C,C的结构简式为:
,B能被新制氢氧化铜氧化、然后酸化生成C,C的结构简式为: ,C和甲醇反应生成2-甲基丙酸甲酯,2-甲基丙酸甲酯发生消去反应生成MMA,D和一氧化碳、甲醇以物质的量之比1:1:1反应恰好生成MMA,则D的结构简式为:CH≡CCH3,结合物质的结构、性质来分析解答.
,C和甲醇反应生成2-甲基丙酸甲酯,2-甲基丙酸甲酯发生消去反应生成MMA,D和一氧化碳、甲醇以物质的量之比1:1:1反应恰好生成MMA,则D的结构简式为:CH≡CCH3,结合物质的结构、性质来分析解答.
解答 解:丙酮和HCN发生加成反应生成A,A的结构简式为:(CH3)2C(OH)CN,A发生消去反应生成CH2=C(CH3)CN,CH2=C(CH3)CN和水反应生成CH2=C(CH3)COOH,CH2=C(CH3)COOH和甲醇反应生成MMA,MMA的结构简式为:CH2=C(CH3)COOCH3,在一定条件下,丙烯和一氧化碳、氢气反应生成B,B的结构简式为: ,B能被新制氢氧化铜氧化、然后酸化生成C,C的结构简式为:
,B能被新制氢氧化铜氧化、然后酸化生成C,C的结构简式为: ,C和甲醇反应生成2-甲基丙酸甲酯,2-甲基丙酸甲酯发生消去反应生成MMA,D和一氧化碳、甲醇以物质的量之比1:1:1反应恰好生成MMA,则D的结构简式为:CH≡CCH3,
,C和甲醇反应生成2-甲基丙酸甲酯,2-甲基丙酸甲酯发生消去反应生成MMA,D和一氧化碳、甲醇以物质的量之比1:1:1反应恰好生成MMA,则D的结构简式为:CH≡CCH3,
(1)2-甲基丙酸甲酯在500℃并有催化剂存在的条件下发生消去反应生成MMA,
故答案为:消去反应;
(2)与2-甲基丙酸甲酯互为同分异构体,且该物质中含有醛基、酯基和手性碳原子,结合其分子式知,该物质中为甲酸酯,则该物质的结构简式为:HCOOCH(CH3)CH2CH3,
故答案为:HCOOCH(CH3)CH2CH3;
(3)通过以上分析知,D的结构简式为:CH≡CCH3,该反应中没有其它副产物生成,所以原子利用率为100%,
故答案为:CH≡CCH3;原子利用率为100%;
(4)MMA和1-丙醇发生取代反应生成甲基丙烯酸丙酯和甲醇,所以该反应的化学方程式为 +CH3CH2CH2OH→
+CH3CH2CH2OH→ +CH3OH,
+CH3OH,
故答案为: +CH3CH2CH2OH→
+CH3CH2CH2OH→ +CH3OH;
+CH3OH;
(5)该反应合成路线为:2-甲基丙烯和一氧化碳、氢气反应生成2,2-二甲基丙醛,2,2-二甲基丙醛和HCN发生加成反应生成 ,
, 在浓硫酸作用下反应生成
在浓硫酸作用下反应生成 ,
, 发生分子间酯化反应生成
发生分子间酯化反应生成 ,
,
故答案为: .
.
点评 本题考查有机物的推断,题目难度中等,本题注意把握有机物官能团的性质和转化,结合反应条件判断可能发生的反应,特别是有机物官能团的性质,为解答该类题目的关键.


科目:高中化学 来源: 题型:选择题

| A. | 气体E呈红棕色,不能直接排放 | |
| B. | 溶液S中所含溶质、沉淀R都可用作药物 | |
| C. | 合金样品中Cu的质量分数为$\frac{a-b-c}{a}$×100% | |
| D. | 合金样品中Al的质量分数为$\frac{9c}{17a}$×100% |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若将等量的硫蒸气和硫固体分别完全燃烧,后者放出热量多 | |
| B. | 由“C(石墨)=C(金刚石)△H=+1.9 kJ•mol-1”可知,金刚石比石墨稳定 | |
| C. | 在101 kPa时,2 g H2完全燃烧生成液态水,放出285.8 kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)═2H2O(l)△H=+285.8 kJ•mol-1 | |
| D. | 在稀溶液中:H++OH-═H2O△H=-57.3 kJ•mol-1,若将含1 mol CH3COOH与含1 mol NaOH的溶液混合,放出的热量小于57.3 kJ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 澄清透明的溶液中:MnO${\;}_{4}^{-}$、SO${\;}_{4}^{2-}$、K+、Fe3+ | |
| B. | 加入铝粉产生氢气的溶液:Na+、K+、SO42-、Cl- | |
| C. | 使pH试纸变红的溶液中:NH4+、Cu2+、SO42-、Cl- | |
| D. | 0.1mol•L-1CH3COONa溶液中:H+、Ca2+、Cl-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用聚合硫酸铁作为净水剂,该处理过程中仅发生了化学变化 | |
| B. | “血液透析”利用了胶体的性质 | |
| C. | 气象环境报告中的“PM2.5”是对一种新分子的描述 | |
| D. | 氢氧化钠可作胃酸的中和剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 制玻璃时会产生CO2 | |
| B. | 生产硅、铝、铜都涉及氧化还原反应 | |
| C. | 制粗硅的反应SiO2+C $\frac{\underline{\;高温\;}}{\;}$Si+CO2↑ | |
| D. | 黄铜矿炼铜产生的SO2可生产硫酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 2KI+Br2=2KBr+I2 | B. | 2AgNO3$\frac{\underline{\;\;△\;\;}}{\;}$2Ag+2NO2↑+O2↑ | ||
| C. | Cu2(OH)2CO3$\frac{\underline{\;\;△\;\;}}{\;}$2CuO+CO2↑+H2O | D. | C+H2O$\frac{\underline{\;\;△\;\;}}{\;}$CO+H2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com