
【题目】现有镁铝合金共3.90克,与500ml 2.00mol/L盐酸(足量)反应,生成的气体在标准状况下体积为4.48L,若反应后所得溶液的体积稀释为1000ml,求:
(1)求镁铝合金中铝的物质的量。
(2)求镁铝合金中镁的质量分数。
(3)求反应后溶液中Cl-的物质的量浓度。
【答案】(1) 0.1mol;(2) 30.8% ;(3) 1mol/L
【解析】本题主要考查关于物质的量的计算。
(1)氢气的物质的量为n(H2)=![]() =
=![]() =0.2mol,
=0.2mol,
Mg+2HCl![]() MgCl2+H2↑,2Al+6HCl
MgCl2+H2↑,2Al+6HCl![]() 2AlCl3+3H2↑,
2AlCl3+3H2↑,
根据题意可得n(Mg)×24g/mol +n(Al)×27g/mol=3.90g和2n(Mg)+3n(Al)=2n(H2)(电子守恒),解得n(Mg)=0.05mol,n(Al)=0.1mol。
(2)镁铝合金中镁的质量为0.05mol×24g/mol=1.2g,镁铝合金中镁的质量分数为1.2/3.90=30.8%。
(3)根据c浓V浓= c稀V稀可得反应后溶液中Cl-的物质的量浓度为(500ml×2.00mol/L)/1000ml=1mol/L。


 53随堂测系列答案
53随堂测系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机化合物的说法正确的是( )
A. 2-甲基丁烷也称异丁烷 B. 由乙烯生成乙醇属于加成反应
C. C4H9Cl有3种同分异构体 D. 糖类和蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表中评价合理的是
选项 | 化学反应及其离子方程式 | 评 价 |
A | NaHSO4溶液与Ba(OH)2溶液反应至 SO42-沉淀完全: 2H++SO42-+Ba2++2OH- = BaSO4↓ + 2H2O | 正 确 |
B | 向碳酸镁溶液中加入足量稀盐酸: CO32-+2H+=CO2↑+H2O | 错误,碳酸镁不应写成离子形式 |
C | 向沸水中滴加饱和的氯化铁溶液至液体变为红褐色: Fe3++3H2O = Fe(OH)3↓+3H+ | 正 确 |
D | NaOH溶液中通入少量CO2反应:OH-+CO2=HCO3- | 正 确 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①Cl2②铝③醋酸(CH3COOH)④CO2⑤H2SO4⑥熔融Ba(OH)2 ⑦氨水⑧稀硝酸⑨Al2(SO4)3固体 ⑩NaHSO4
(1)按物质的分类方法填写表格的空白处:
属于非电解质的是__________;属于弱电解质的是________;属于强电解质的是__________;能导电的是____________。
(2)写出③溶于水时的电离方程式________________________________________。
(3)实验室常用高锰酸钾固体与浓盐酸在常温下反应来快速制备少量①。反应方程式为: KMnO4 + HCl(浓) —— KCl + MnCl2 + Cl2↑ + H2O(未配平)
配平上述反应并用双线桥法标出反应中电子转移的方向和数目:____________________
KMnO4 + HCl(浓) —— KCl + MnCl2 + Cl2↑ + H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)![]() 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
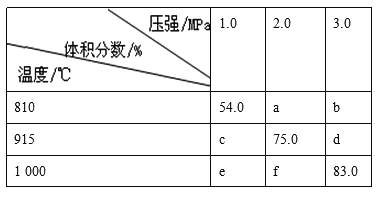
①b<f ②915℃、2.0 MPa时E的转化率为60% ③该反应是△S>0 ④K(1000℃)>K(810℃)
上述①~④中正确的有( )
A. 4个 B. 3个 C. 2个 D. 1个
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列括号中的分离方法运用得当的是
A. 植物油和水(蒸馏)
B. 水溶液中的食盐和碘(分液)
C. CaCO3和CaCl2(溶解、过滤、蒸发)
D. 自来水中的杂质(萃取)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生进行蔗糖的水解实验,并检验水解产物中是否含有葡萄糖。他的操作如下:取少量纯蔗糖加配成溶液;在蔗糖溶液中加入3~5滴稀硫酸;将混合液煮沸几分钟、冷却;在冷却后的溶液中加入银氨,在水浴中加热。实验结果没有银镜产生。其原因是( )
A. 蔗糖尚未水解 B. 蔗糖水解的产物中没有葡萄糖
C. 加热时间不够 D. 煮沸后的溶液中没有加碱,以中和作催化剂的酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学组装了如图所示的电化学装置,则下列说法正确的是( )

A. 图中甲池为原电池装置,Cu电极发生还原反应
B. 实验过程中,甲池左侧烧杯中NO3-的浓度不变
C. 若甲池中Ag电极质量增加5.4g时,乙池某电极析出1.6g金属,则乙中的某盐溶液可能是AgNO3溶液
D. 若用铜制U形物代替“盐桥”,工作一段时间后取出U形物称量,质量会减小
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com