
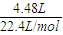 =0.2mol,
=0.2mol,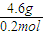 =23g/mol,
=23g/mol,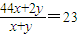 ,x:y=1:1,
,x:y=1:1,

 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

| 1 |
| 2 |
| 1 |
| 2 |
| a |
| 56 |
| b |
| 22.4 |
| a |
| 56 |
| b |
| 22.4 |
查看答案和解析>>
科目:高中化学 来源: 题型:
(1) 相同物质的量的O2和O3,所含分子数目之比为_________,所含O的物质的量之比为_________。
(2) 在标准状况下,4 g H2、11.2 L O2、1 mol H2O中,含原子数最多的是______,体积最小的是_______。
(3) 标况下,将224L的HCl气体溶于835ml(ρ=1g/cm3)的水中,所得盐酸的密度为1.2g/cm3, 该盐酸的物质的量浓度___________
(4) 某气体物质质量为6.4 g,含有6.02×1022个分子,则该气体的相对分子质量为__________
(5)Na2CO3的摩尔质量是____________,0.5mol Na2CO3的质量是____________,含有________mol Na+, ______mol CO3 2-,Na+的个数约为___________;若将其溶于水,配成250mL的溶液,则该溶液溶质的物质的量浓度为_____________;若向溶液中加入过量的稀盐酸,产生的气体体积为(标况下)__________.
查看答案和解析>>
科目:高中化学 来源:2009-2010学年河南省郑州市高一(上)期末化学试卷(解析版) 题型:选择题
查看答案和解析>>
科目:高中化学 来源:2012届河北省唐山一中高三上学期期中考试化学试卷 题型:单选题
下列叙述中完全正确的一组是
①常温常压下,1 mol甲基所含的电子数为10NA;②由Cu、Zn和稀硫酸组成的原电池工作时,若Cu极生成0.2g H2,则电路通过电子0.2NA;③在标准状况下,11.2 L NO与11.2 L O2 混合后气体分子数为0.75NA;④常温常压下,16 g O3所含的原子数为NA;⑤1 mol C10H22分子中共价键总数为31 NA;⑥1 mol Cl2发生反应时,转移的电子数一定是2 NA;
⑦标准状况下,22.4 L水中含分子数为NA
| A.①②③④⑤ | B.②④⑤⑥⑦ | C.②④⑤ | D.①②⑤ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com